时间:2019-06-25 23:32:29
1、选择题 Al3+ + 3H2O Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是
Al(OH)3 + 3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH值增大,应采取的措施是
A.加热
B.加适量NaOH溶液
C.通入氯化氢气体
D.加入固体三氯化铝
参考答案:B
本题解析:水解吸热,加热促进水解,溶液的pH降低,A不正确;氢氧化钠能结合氢离子,降低氢离子的浓度,常见水解,B正确;C中增大氢离子的浓度,抑制水解,不正确;D中氧化铝不溶于水,对水解平衡几乎没有影响,不正确,答案选B。
考点:考查外界条件对水解平衡的影响
点评:该题是中等难度试题的考查,也是高考中的常见题型和考点。该题的关键是明确氯化铝的水解平衡特点,然后结合题意灵活运用勒夏特列原理即可,难度不大。
本题难度:一般
2、填空题 (1)AgNO3的水溶液呈酸性的原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)在25℃下,将a mol・L-1的氨水与0.01 mol・L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有 ,其浓度由大到小的顺序为 ,氨水的浓度a 0.01 mol・L-1(填“>”、“<”或“=”)。
(3)用已知浓度的NaOH标准溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
A.未用标准液润洗碱式滴定管;
B.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
D.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
参考答案:⑴Ag++ H2O 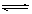 AgOH +H+ 抑制
AgOH +H+ 抑制
⑵OH-、H+、NH4+、Cl- c(Cl-)=c(NH4+)>c(H+)=c(OH-) >
⑶AB
本题解析:(1)银离子在水溶液中可发生水解,有氢离子生成,所以溶液显酸性。硝酸中会存在大量的氢离子,所以可以抑制硝酸银的水解(2)产物是氯化铵和水,所以溶液中会存在氢氧根离子、氢离子、铵根离子、氯离子。主要产物是氯化铵,而铵根离子会发生水解生成氢氧根离子,而从题意可知溶液呈中性,所以排序为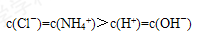
考点:盐类水解相关知识的应用
本题难度:一般
3、选择题 常温常压下,将a mol CO2气体通入1L bmol/L的NaOH溶液中,下列对所得溶液的描述不正确的是
A.当a=2b时,随着CO2气体的通入,溶液中由水电离出的c(H+)有如图变化关系
B.当a=b时,所得溶液中存在:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
C.当2a=b时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
D.当1/2<a/b<1时,所得溶液中一定存在:c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
参考答案:D
本题解析:A、当a=2b时,二氧化碳过量,随着CO2气体的通入,先发生CO2+2NaOH=Na2CO3+H2O,生成的碳酸钠水解,促进水的电离,而氢氧化钠溶液中,氢氧根离子抑制水的电离,所以水电离产生的氢离子浓度增大,后发生Na2CO3+H2O+ CO2="2" NaHCO3,碳酸氢钠的水解程度比碳酸钠水解程度弱,所以促进水电离的程度减小,氢离子浓度又降低,符合图像,正确;B、当a=b时,所得溶液是碳酸氢钠溶液,根据质子守恒定律,水电离产生的氢离子等于氢氧根离子浓度,水电离产生的氢离子一部分被碳酸氢根离子结合生成碳酸分子,同时碳酸氢根离子电离产生氢离子和碳酸根离子,所以溶液中c(OH-)= c(H+)+c(H2CO3)- c(CO32-),即c(OH-)+c(CO32-)=c(H+)+c(H2CO3),正确;C、当2a=b时,所得溶液为碳酸钠溶液,碳酸根离子水解使溶液呈碱性,所以c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),正确;D、当1/2<a/b<1时,所得溶液为碳酸钠和碳酸氢钠的混合液,若为碳酸氢钠溶液,则一定存在c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3),错误,答案选D。
考点:考查二氧化碳与氢氧化钠溶液反应的判断,离子浓度关系的判断
本题难度:一般
4、填空题 (14分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
| 实验 编号 | HA物质的量浓度(mol・L-1) | NaOH物质的量浓度(mol・L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
参考答案:(1)a=7;a>7 (2)否;c(A-)=c(Na+) (3)弱 c(Na+)>c(A-)>c(OH-)>c(H+) (4)10-5
本题解析:(1)如果HA是强酸,则等体积、等物质的量浓度的HA与NaOH混合,溶液呈中性,如果HA是弱酸,则等体积、等物质的量浓度的HA与NaOH混合,溶液呈酸性。
(2)如果HA为弱酸,与等浓度,等体积的NaOH溶液反应后,溶液呈中性,则需要酸过量,所以c大于0.2,根据电荷守恒:c(H+)+ c(Na+)= c(OH-)+ c(A-),若c(H+)= c(OH-)则c(Na+)= c(A-)。
(3)根据丙可知,酸过量,反应后的溶液呈碱性,说明酸是弱酸。根据电荷守恒:c(H+)+ c(Na+)= c(OH-)+ c(A-),c(H+)< c(OH-),溶质电离出来的离子大于水电离出来的离子,所以溶液中离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+)。
(4)酸和碱等体积等浓度混合,则恰好完全反应,溶液显碱性,说明生成了强碱弱酸盐。溶液中的H+都是由水电离出来的,所以水电离出来的c(H+)= c(OH-)=10-5mol/L。
考点:盐类水解
点评:本题属于盐类水解的综合性习题,是高考中的热点习题。计算水电离出来的离子,要考虑溶液中的H+或OH-是由谁电离出来的,再根据Kw去求。
本题难度:困难
5、选择题 下列关于pH=12的Na2CO3溶液说法正确的是
A.升高溶液温度,溶液pH增大
B.c(Na+) +c(H+)=c(CO32-)+ c(HCO3-)+ c(OH-)
C.溶液中c(OH-)>c(HCO3-)> c(H+)
D.2c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3)
参考答案:AC
本题解析:碳酸钠是强碱弱酸盐,少部分碳酸根离子能够水解,即CO32―+H2O HCO3―+OH―,该水解反应是吸热反应,升高温度,促进碳酸根离子水解,氢氧根离子浓度增大,溶液的pH增大,故A选项正确;B项,违反电荷守恒原理,碳酸钠溶液中存在Na+、H+、CO32-、HCO3-、OH-,由于溶液呈电中性,则阳离子的正电荷总浓度等于阴离子的负电荷总浓度,即c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故B选项错误;碳酸根离子的水解分两步进行,CO32―+H2O
HCO3―+OH―,该水解反应是吸热反应,升高温度,促进碳酸根离子水解,氢氧根离子浓度增大,溶液的pH增大,故A选项正确;B项,违反电荷守恒原理,碳酸钠溶液中存在Na+、H+、CO32-、HCO3-、OH-,由于溶液呈电中性,则阳离子的正电荷总浓度等于阴离子的负电荷总浓度,即c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故B选项错误;碳酸根离子的水解分两步进行,CO32―+H2O HCO3―+OH―,HCO3―+H2O
HCO3―+OH―,HCO3―+H2O H2CO3+OH―,第一步水解程度大于第二步水解,碳酸钠溶液呈碱性,则溶液中c(OH-)>c(HCO3-)> c(H+),故C选项正确;D项,违反物料守恒原理,因为碳酸钠中钠离子是碳酸根离子的2倍,则平衡时溶液中c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D选项错误。
H2CO3+OH―,第一步水解程度大于第二步水解,碳酸钠溶液呈碱性,则溶液中c(OH-)>c(HCO3-)> c(H+),故C选项正确;D项,违反物料守恒原理,因为碳酸钠中钠离子是碳酸根离子的2倍,则平衡时溶液中c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D选项错误。
考点:考查水溶液中粒子浓度大小关系,涉及酸与盐溶液中电荷守恒关系式、溶液pH、水的离子积、电离平衡移动、溶液的酸碱性、盐与盐溶液中物料守恒关系式等。
本题难度:困难