ʱ��:2019-06-25 22:33:00
1������� ��ʽ̼��þ�ж��ֲ�ͬ����ɣ��� ��
��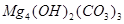 ��
�� �ȡ��������һ���ⶨ��ʽ̼��þ��ɵ�ʵ�鷽��������
�ȡ��������һ���ⶨ��ʽ̼��þ��ɵ�ʵ�鷽��������
��1���ⶨԭ��
��2���ⶨʵ���װ��ͼ
��3���������衣
��ʹ�õ��������Լ�����Ʒ���£�
��������ƽ�������룩�����Թܣ������ж̲����ܵ���Ƥ�������ƾ��ơ�ϴ��ƿ�����θ���ܣ������ж̲����ܵ���Ƥ����������̨�����С��dzס�
�Լ�����ʽ̼��þ����״����Ũ���ᡢʯ��ˮ����ˮ�Ȼ��ơ���ʯ�ҡ�
�����������������Ƥ�ܡ����ɼС�
ע�⣺�������������Լ�ֻ��Ӧ�����е�һ���֡����������Լ�����Ʒ���������ޡ�
�ο��𰸣���1��ͨ���ⶨMgO��CO2��H2O�����ʵ���֮�����ⶨ��ʽ̼��þ����ɡ�
��2���ⶨʵ���װ������ͼ��ʾ�� ?
?
��3����������
�� ��װ�ð���ͼ���Ӻú��װ�õ�������
�� ��ȡһ������W1g����Ʒ�ڴ��Թ���
�� ���ȣ�����Ʒ��ȫ�ֽ�
�� ʵ���������ϴ��ƿ����ܵ����أ���ΪW2��W3��
�� ����MgO��CO2��H2O�����ʵ���֮��Ϊ
n��MgO����n��CO2����n��H2O��= :
: :
: ?ȷ����ʽ̼��þ����ɡ�
?ȷ����ʽ̼��þ����ɡ�
���������
���������������ⶨ��ʽ̼��þ��ɵ�ʵ�鷽����ơ�
�����⡿�ɼ��ȼ�ʽ̼��þ��ͨ���ⶨ���ɵ�MgO��CO2��H2O�����ʵ���֮����ȷ����ʽ̼��þ����ɡ���Ũ��������H2O������Ũ�������ص��������ˮ�����ʵ������ü�ʯ������CO2�����ݼ�ʯ�ҵ����أ�ȷ��CO2���ʵ�����
�����Ѷȣ���
2��ѡ���� ��������ʵ����Ƽ��й��������ý��۲���ȷ����
A?B?C?D
| ʵ �� | ʵ������ | �� �� | |||||||||||||||
| A | ���ձ��������������ݣ��ұ��ձ���ͭ���������� | ��ԣ�Al��Fe��Cu | |||||||||||||||
| B | �������Ϊ��ɫ���ұ�����Ϊ��ɫ | �����ԣ�Cl2��Br2��I2 | |||||||||||||||
| C | ��ɫ�����ȱ�Ϊ����ɫ�����Ϊ��ɫ��Ag2S�� | �ܽ��� ��AgCl��AgBr��Ag2S | |||||||||||||||
| D | ��ƿ��������������ձ���Һ������ | ���ԣ�HCl��H2CO3��H2SiO3 �ο��𰸣�BD ��������� �����Ѷȣ��� 3��ʵ���� ҽ���Ȼ��ƿ������������ơ�������������ҩ��Թ�ҵ̼��ƣ��������� �ο��𰸣���1��ȡ�����ϲ���Һ���μ�KSCN��Һ����������Ѫ��ɫ�������Fe(OH)3������ȫ ��������� �����Ѷȣ�һ�� 4��ѡ���� ���в��ܴﵽʵ��Ŀ�ĵ���
�ο��𰸣�C ���������A�����ݽ����������������ŵ���Ⱥ�˳������жϽ������ǿ����ͭ�����ȷŵ磬����ͭ��Ծ�������ȷ��B�����ݡ�Խ��Խˮ�⡱����ˮ����ɣ���ۺ����������Խ�����Ӧ���������ˮ��̶�Խ��pHԽ��һ���Ƴ���ǽ�����Խ������ȷ��C����pH��ֽ�ⶨŨ��Ϊ0��1mol��L��1NaClO��������ֽƯ�ף�ʵ��ﲻ��Ŀ�ģ�����D�����Ƶ�һ���������ı�Ũ�ȣ��ܹ��ﵽʵ��Ŀ�ģ���ȷ�� �����Ѷȣ�һ�� 5������� ij��γ�С������50mL?NaOH��Һ����CO2���壬�Ʊ�Na2CO3��Һ��Ϊ�˷�ֹͨ�������CO2��������NaHCO3�����������ʵ�鲽�裺 �ο��𰸣���1��̼�������ܺ��������Ʒ�Ӧ����̼���ƺ�ˮ����Ӧ���ӷ���ʽΪHCO3-+OH-�TCO32-+H2O�� ��������� �����Ѷȣ�һ�� |