时间:2019-06-25 22:31:57
1、实验题 (6分)某课外小组同学设计了下列实验装置,通过测定某些装置中试剂的质量变化,探究某孔雀石[化学式为aCuCO3・bCu(OH)2,a、b为正整数]中各元素的质量关系。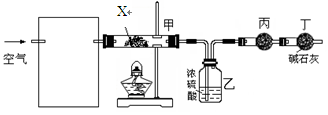
①为使数据准确,还需补充装置,请你在方框内绘出装置图并写出试剂名称;(注:碱石灰可看作烧碱和生石灰的混合物)
②向装置中鼓入空气的目的是__ ________?;
丙装置中药品的名称为________?,
实验时,该药品未见明显变化,证明____________________________________________;
③连续两次加热、鼓气、冷却、称量甲装置的质量,质量差不超过0.1 g,判断该孔雀石已完全分解。
④更精确的测定得出如下数据:孔雀石受热后完全分解,固体由16.52 g变为12.00 g,装置乙增重1.44 g。写出该孔雀石的化学式________________________。
参考答案:①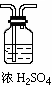 或
或
(多加NaOH溶液洗气瓶扣1分,共1分)
②将X分解产生的水蒸气送入盛有浓硫酸的洗气瓶中(1分) ;无水硫酸铜(1分);
;无水硫酸铜(1分);
X分解产生的水蒸气全部被浓硫酸吸收(1分)
7CuCO3・8Cu (OH)2 或Cu15(OH)16(CO3)7或15CuO・7CO2 ・8H2O (2分)
本题解析:略
本题难度:简单
2、实验题 某烧碱样品含有少量不与酸作用的杂质,为了滴定其纯度,进行以下滴定操作:
A.在250mL的容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中滴加几滴酚酞做指示剂
C.在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为C的标准盐酸溶液装入酸式滴定管,调整液面记下开始读数为V1mL
E.在锥形瓶下垫一张白纸,滴定至红色刚好消失为止,且颜色不再变化,记下读数V2mL
回答下列问题:
(1)正确操作步骤的顺序是(填字母):??→?→??→ D →?。
(2)操作E中的锥形瓶下垫一张白纸的作用是?。
(3)操作D中液面应调整到?,尖嘴部分应?。
(4)某学生实验时把锥形瓶用烧碱溶液润洗,使测定的浓度?(填“偏高”、“偏低”或“无影响”),原因是?。?
(5)当用酸滴定碱时,下列操作中使测定结果(碱的浓度)偏低的是?。
A.酸式滴定管滴至终点时,俯视读数?
B.碱液移入锥形瓶后,加了10 ml蒸馏水再滴定
C.酸式滴定管用蒸馏水润洗后,未用操作液润洗
D.酸式滴定管注入酸液后,尖嘴留有气泡,开始滴定
(6)该烧碱样品纯度的计算式为?。?
参考答案:(1)C、A、B、E;?(2)便于观察溶液颜色的变化。
(3)“0”或“0”以下某一刻度;充满溶液,无气泡;
(4)偏高;该错误操作将导致多消耗标准酸溶液;
(5)A
(6)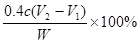
本题解析:(1)考查中和滴定实验操作。
(2)白纸能使溶液颜色的变化更清晰,便于观察溶液颜色的变化。
(3)滴定管的刻度是自上而下逐渐增大的,所以液面应该调节到“0”或“0”以下某一刻度。滴定管的尖嘴部分应该是充满溶液,无气泡。
(4)锥形瓶用烧碱溶液润洗,则锥形瓶内碱的物质的量增加,消耗酸的体积增大,测定结果偏高。
(5)俯视读数,则读数偏小,即酸的体积偏小,测定结果偏低。将碱液稀释,并没有改变OH-的物质的量,所以测定结果不变。没有用标准液润洗,则相当于稀释了酸,因此消耗酸的将偏大,测定结果偏高。尖嘴留有气泡,则说明起始读数偏小,因此测定结果偏高,答案选A。
(6)消耗酸的体积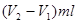 ,所以原样品中氢氧化钠的质量是
,所以原样品中氢氧化钠的质量是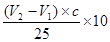 ,所以烧碱样品纯度的计算式为
,所以烧碱样品纯度的计算式为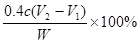 。
。
本题难度:一般
3、实验题 试用下列试剂:酚酞试液、石蕊试液、稀氨水、氯化铵晶体、浓盐酸、熟石灰粉末、醋酸铵晶体和蒸馏水。根据①弱碱在水中存在电离平衡;②弱碱的阳离子破坏水的电离平衡,这两种平衡移动均会引起指示剂颜色变化,分别选用上述试剂,设计两个实验证明NH3・H2O是弱碱,简述实验方法和现象。 (以离子方程式和简要文字说明)。
参考答案:(1)取少量稀氨水,滴入酚酞试液,溶液呈红色,再加入醋酸铵晶体,溶液红色变浅,
NH3・H2O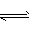 NH4++ OH -,CH3COONH4
NH4++ OH -,CH3COONH4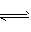 CH3 COO-+ NH4+。
CH3 COO-+ NH4+。
(2)取少量NH4Cl晶体,加蒸馏水溶解,滴入紫色石蕊试液,溶液变红色,NH4++ H2O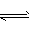 NH3・H2O+H+
NH3・H2O+H+
本题解析:
本题难度:一般
4、选择题 下图是制取、洗涤并测量生成气体体积的装置示意图,利用该装置进行下表所列实验,能达到实验目的的是 (?)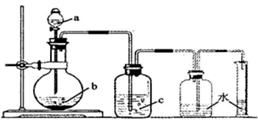
 物质 物质实验 | a(液体) | b(固体) | c(液体) |
| A | 稀硫酸 | 锌粒 | 浓H2SO4 |
| B | 稀硫酸 | 石灰石 | 浓H2SO4 |
| C | 浓硫酸 | Cu片 | NaOH溶液 |
| D | 稀HNO3 | Cu片 | H2O |
参考答案:A
本题解析:略
本题难度:简单
5、实验题 如图所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化时的颜色变化。 
(1)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(2)简述生成Fe(OH)2的操作过程__________。
(3)实验完毕,打开b处活塞,放入一部分空气,此时B瓶中发生的反应为______________。
(4)下列各图示中_____能较长时间看到Fe(OH)2白色沉淀。 
参考答案:(1)打开
(2)关闭活塞a,使FeSO4溶液压入B中进行反应
(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(4)①②④
本题解析:
本题难度:一般