ʱ��:2019-06-25 22:07:05
1��ѡ���� �ڳ����£�ȡ������ˮ��ʪ��pH��ֽ���ϸ��չ淶��ʵ������������ⶨ��ˮ�������H+Ũ��Ϊ
1�� 10-10 mol/L����Һ��pH�����ܻ���ֲⶨ������˵������ȷ����
[? ]
A���ⶨ���ƫ��
B���ⶨ���ƫС
C���ⶨ��������
D����ȷ���ⶨ�����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ����ʵ������������?
[? ]
A����ҩ��ȡ������Na2SO4���� ?
B���ý�ͷ�ιܵμ�����NaCl��Һ
C������ʢ��2/3���K2SO4��Һ���Թ� ?
D����10?mL��Ͳ��ȡ8?mL1.?0?mol/L?NaOH��Һ
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� �����й�ʵ���������˵����ȷ���ǣ�?��
A�����Ʊ���ϩ��ʵ���У�Ϊ�˷�ֹ��Ӧ�������������ʱӦʹ�¶�Ѹ��������170OC
B���ֱ�����֧ʢ�������������Թ��м�������������Һ��ϡ���ᡢˮ������ˮԡ�м��ȣ�����������ζɢʧ���ٶȰ��������ơ�ˮ��ϡ�����˳�����μ���
C�������������NaOH��Һ�У�����ַ�Ӧ�ټ���AgNO3��Һ����dz��ɫ��������
D������ϡ��Һ�У�ͨ������������̼���壬��Һ������̼����
�ο��𰸣�A
���������
��ȷ�𰸣�A
A��140��ʱ�������ѣ�B��ˮ���ٶ��ɿ쵽��˳��Ϊ���������ơ�ϡ���ᡢˮ��C����AgNO3֮ǰ��Ӧ�ȼ�HNO3��NaOH�кͣ�D�����ԣ�C6H5OH����HCO3�D��Ӧ����NaHCO3.
�����Ѷȣ�һ��
4��ʵ���� ��16�֣�ʵ���ǽ��л�ѧ�о�����Ҫ�ֶ�֮һ����ش��������⣺
��1������ʵ��������������____________________����д��ţ���
a. ��ֽ�����Թ���װ��ĩ״ҩƷʱ���Թ�Ӧ�Ⱥ����ֱ��
b. ��ȡ�������ƹ���ʱ��Ӧ���������ƹ���ֱ�ӷ�����������ڣ��ұ����̷�����
c. �� �ܡ��ձ�����Ͳ������ƿ�������þƾ���ֱ�Ӽ���
d.����ֽ������������ʱ����������ֽ��ˮ��ϴ������۲���ֽ��ɫ�ı仯
e.��������ζʱ��Ӧȡһƿʢ������ļ���ƿ���Դ���Ƭ�����������ȵ���ƿ���ȶ���ʹ������������Ʈ���ǿף�����ζ
��2��ʵ������Ҫ450mL 0.1mol��L-1NaOH��Һ��500mL 0.5 mol��L-1������Һ����ش���
������:
������ͼ��ʾ�����У�����������Һ�϶�����Ҫ����_________������ţ�����ͼ�����������⣬����������Һ����Ҫ�IJ���������?��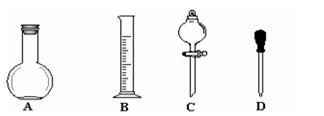
��������ƿ��ʹ�÷����У����в�����ȷ����____________����д��ţ���
a��ʹ������ƿǰ�����Ƿ�©ˮ
b������ƿ��ˮϴ�������ô�����Һϴ��
c��������Һʱ����������Һ�壬����Ͳȡ�����ò���������ע������ƿ�У�Ȼ�������ˮ��
d���Ǻ�ƿ������ʳָ��סƿ������һֻ����סƿ�ף�������ƿ������ת��Σ�ҡ�ȡ�
������450 mL 0.1 mol��L-1 NaOH��Һ��ʵ�鲽�����£�
a.����Ӧ��ȡ�������ƹ��������Ϊ________g��
b.�����������ƹ��塣
c.���ձ��е���Һע������ƿ��������������ˮϴ���ձ��ڱ�2~3�Σ�ϴ��ҺҲע����
��ƿ��
d.������������ˮ�ܽ�����õ��������ƹ��壬��ȴ��
e.�Ǻ�ƿ�����������µߵ���ҡ�ȡ�
f.����������ƿ�м�����ˮ���̶�����1~2cmʱ�����ý�ͷ�ιܵμ�����ˮ����Һ����
�̶������С�
�����������ȷ����˳��Ϊ_______________________������ű�ʾ����
�ܸ��ݼ����֪��������Ͳ��ȡ��������Ϊ98%���ܶ�Ϊ1.84g/cm3��Ũ��������Ϊ?mL�����ʵ������15mL��20mL��50mL��Ͳ��Ӧѡ��?mL��Ͳ��á�
�ο��𰸣���16�֣���1�� bcd��2�֣�
��2���� A C��2�֣�?�ձ�����������500mL����ƿ��2�֣�ÿ��һ�ֿ�1�֣�
�� ?ad��2�֣�?��2.0��2�֣� ?abdcfe��2�֣�
��13.6��2�֣�?15��2�֣�
�������������ʵ�������������Һ������
��1��a����ȷ��
b:����NaOH��ǿ��ʴ�Լ���ˮ�ԣ�һ����С�ձ�ʢ�ź�������ƽ����
c:�Թܿ���ֱ�Ӽ���
d:�ֲ���ֱ�ӽӴ���ֽ���Է���Ⱦ
e����ȷ
��2�������ƻ�ϡ����Һ�Ĺ����в���Ҫƽ����ƿ����Һ©��������Ҫ�����������ձ�����������500mL����ƿ
��a����ȷ
b:����ƿֻ��Ҫ��ˮϴ�Ӹɾ����ɣ������ô�������Һ��ϴ
c:�������ܽ���廹��ϡ��Ũ��Һ����Ӧ�����ձ����У�����ƿֻ������������Һ
d����ȷ
�������������ƹ����������0.5��0.1��40=2.0g
��ȷ��������Һ�IJ���Ϊ�����㡢�������ܽ⡢ϴ�ӡ����ݡ�ҡ��
��Ũ��������Ϊ��V��1.84��98%/98=0.5��0.5����V=13.6ml
Ӧѡ���ݻ��Դ���13.6ml����Ͳ����15ml
�����Ѷȣ�һ��
5��ѡ���� ͭ���������緢�ֺ�ʹ�õĽ���֮һ��ͭ����Ͻ����;�㷺����ͭ�к�����������п����������������ʣ���ҵ�Ͽ��õ�ⷨ������ͭ�Ƶô�ͭ������������ȷ����(��֪��������Fe2+��Ni2+��Cu2+)
A.��ͭ����������缫��Ӧʽ��Cu2++2e-��Cu
B.�������У��������Һ��c(Cu2+)����
C.���������ϻ����м�������Fe��Ni
D.�����������������������ȹ����
�ο��𰸣�D
���������
�����Ѷȣ�����