时间:2019-06-25 21:43:34
1、选择题 某可逆反应正向反应过程中能量变化如图所示,下列说法正确的是(? )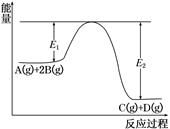
A.该反应为吸热反应
B.当反应达到平衡时,降低温度,A的转化率减小
C.升高温度平衡常数K增大;压强增大,平衡向正反应方向移动
D.加入催化剂,反应速率增大,E1减小,E2减小,反应热不变
2、选择题 一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是( )
A.以X浓度变化表示的反应速率为0.001mol/(L?s)
B.将容器体积变为20L,Z的平衡浓度变为原来的
| 1 2 |
3、计算题 一定温度下,在密闭容器中,发生反应: 2NO2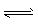 2NO+O2,经过一定时间后,测得混合气中NO2浓度为0.06 mol・L-1, O2的浓度为0.12 mol・L-1,且各物质的浓度不再发生变化。
2NO+O2,经过一定时间后,测得混合气中NO2浓度为0.06 mol・L-1, O2的浓度为0.12 mol・L-1,且各物质的浓度不再发生变化。
求:
(1)NO2的起始浓度? ;
(2)此时NO2的转化率? 。
4、计算题 将相同物质的量的SO3充入下面的两个容器中,已知甲容器有活塞可以上下移动,乙容器体积固定,在相同的温度、压强下开始发生反应:2SO3(g) ?2SO2(g)+O2(g),在反应过程中维持体系温度不变。
?2SO2(g)+O2(g),在反应过程中维持体系温度不变。
(1)求达到平衡状态时SO3气体的转化率的大小关系? 图2-2
图2-2
(2)达到平衡状态时分别充入一定量的Ar气,平衡是否会移动?会怎样移动?
5、选择题 在一密闭容器内发生氨分解反应:2NH3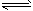 N2+3H2。已知NH3起始浓度是2.6 mol・L-1,4s末为1.0
N2+3H2。已知NH3起始浓度是2.6 mol・L-1,4s末为1.0
mol・L-1,若用NH3的浓度变化来表示此反应的速率,则v(NH3)应为
[? ]