时间:2019-06-25 21:07:15
1、选择题 200mL0.1 mol·L-1CH3COOH与200mL0.1 mol·L-1NaOH溶液混合后,离子浓度关系正确的是
A.c(Na+) = c(CH3COO-)+ c(CH3COOH)
B.c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C.c(Na+)+ c(OH-)= c(CH3COO-)+ c(H+)
D.c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
参考答案:A
本题解析:200mL0.1 mol·L-1CH3COOH与200mL0.1 mol·L-1NaOH溶液混合,恰好生成醋酸钠溶液,则溶液呈碱性,所以c(Na+)>c(CH3COO-)>c(OH-) > c(H+),B、D错误;根据电荷守恒,则c(Na+)+ c(H+) = c(CH3COO-)+ c(OH-),C错误;根据物料守恒,则c(Na+) = c(CH3COO-)+ c(CH3COOH),A正确,答案选A。
考点:考查酸碱混合的判断,离子浓度的关系判断
本题难度:一般
2、填空题 (共8分)(1)Fe(NO3)3的水溶液呈 ___ (填“酸”、“中”、“碱”)性,原因
是(用离子方程式表示): 。
实验室在配制Fe(NO3)3的溶液时,常将Fe(NO3)3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
参考答案:(1)酸; Fe3+ + 3H2O 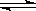 Fe(OH)3 + 3H+;抑制;
Fe(OH)3 + 3H+;抑制;
(2) 氢氧化钠固体(或NaOH)
本题解析:考查盐类水解的应用。
(1)硝酸铁是强酸弱碱盐,铁离子水解,溶液显酸性,水解方程式是 Fe3+ + 3H2O 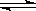 Fe(OH)3 + 3H+;因此在配制硝酸铁溶液时,先将Fe(NO3)3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,目的就是抑制铁离子水解的。
Fe(OH)3 + 3H+;因此在配制硝酸铁溶液时,先将Fe(NO3)3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,目的就是抑制铁离子水解的。
(2)硫化钠时强碱弱酸盐,硫离子水解,溶液显碱性。所以在配制硫化钠溶液时,为了防止发生水解,可以加入少量的氢氧化钠固体以抑制硫离子水解。
本题难度:一般
3、选择题 常温下下列有关CH3COONa溶液中的关系式不正确的是 ( )
A.C((H +)>1.0×10-7mol/L
B.C(CH3COOˉ) +C(OHˉ)=" C(Na" +)+C(H +)
C.C(CH3COOˉ)+C(CH3COOH) ="C(Na" +)
D.C(OHˉ)= C(CH3COOH) +C(H +)
参考答案:A
本题解析:醋酸钠为强碱弱酸盐,水解呈碱性。故A错误。B、电荷守恒,C、物料守恒,D、质子守恒。
本题难度:一般
4、填空题 (10分)按要求完成以下内容:
(1)Fe2(SO4)3水溶液呈________性,原因是(用离子方程式表示):_________________________;实验室在配制Fe2(SO4)3溶液时,需要加入________来抑制水解。
(2)有三瓶pH均为2的盐酸、硫酸溶液、醋酸溶液。
①设三种溶液的物质的量浓度依次为c1、c2、c3,则它们之间由小到大的顺序为______(用“>”“<”或“=”表示,下同)。
②取同体积的三种酸溶液,分别加入足量锌,反应开始产生H2的速率依次为v1、v2、v3,则它们之间的关系是_____________________;
(3)某温度下,水的离子积常数KW=10-14。该温度下,将pH=4的H2SO4溶液与pH=9的NaOH溶液混合并保持恒温,欲使混合溶液的pH=7,则稀硫酸与NaOH溶液的体积比为____________。
参考答案:(1)酸性, Fe3+ + 3H2O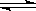 Fe(OH)3 + 3H+ ,稀硫酸 (2)①c2<c1<c3②v1=v2=v3(3)1
Fe(OH)3 + 3H+ ,稀硫酸 (2)①c2<c1<c3②v1=v2=v3(3)1
本题解析:
本题难度:一般
5、填空题 (12分)(1)将一定量氨气通入盐酸中,溶液pH恰好为7(25 ℃),则氨的物质的量_____(填“<”、“=”或“>”)盐酸中HCl的物质的量;溶液中c(NH4+)_____c(Cl-)。
(2)向同体积同物质的量浓度的盐酸和氯化铵溶液中加入等质量的镁粉,镁完全反应后,盐酸放出气体的体积_____氯化铵溶液放出气体的体积。
(3)向盐酸中通入NH3至恰好完全反应时,所得溶液由H2O电离出来的c(H+)比纯水电离出来的c(H+)_____(填“大”、“小”或“相等”)。
参考答案:⑴>(3分) =(3分) ⑵< (3分) ⑶大(3分)
本题解析:(1)如果氨气和盐酸刚好完全反应生成NH4Cl,NH4Cl溶液显酸性,溶液要显中性,氨气应该过量,所以氨气的物质的量大于盐酸的物质的量;根据电荷守恒:c(NH4+) +c(H+)= c(Cl-) +c(OH-),溶液显中性则c(OH-)= c(H+),那么c(NH4+)=c(Cl-)。(2)盐酸和氯化铵溶液与镁粉反应方程式分别为:Mg+2HCl= MgCl2 +H2↑,Mg + 2NH4Cl==MgCl2 + 2NH3 ↑+ H2↑,可以看出盐酸反应产生的气体较少(3)如果氨气和盐酸刚好完全反应生成NH4Cl,NH4+会发生水解,就促进了水的电离,故NH4Cl溶液中水电离出来的c(H+)比纯水中的要大。
考点:盐类水解和溶液中离子浓度的大小比较。
本题难度:一般