时间:2019-05-30 05:13:21
1、填空题 物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种。请根据所学化学知识回答下列问题:
(1)A为0.1 mol・L-1的(NH4)2SO4溶液,在该溶液中离子浓度由大到小的顺序为_______。
(2)B为0.1 mol・L-1的NaHCO3溶液,NaHCO3在该溶液中存在的平衡有(用离子方程式表示)____________________________________。
(3)D为含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:AgCl(s) Ag+(aq)+Cl-(aq) 在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol・L-1 AgNO3溶液 ③100 mL 0.1 mol・L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为__________________(填序号),此时溶液②中Cl-物质的量浓度为__________________。
Ag+(aq)+Cl-(aq) 在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol・L-1 AgNO3溶液 ③100 mL 0.1 mol・L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为__________________(填序号),此时溶液②中Cl-物质的量浓度为__________________。
参考答案:(8分) (每空2分)
(1)c(NH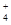 )>c(SO
)>c(SO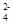 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
(2)HCO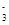
 H++CO
H++CO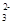 ;HCO
;HCO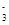 +H2O
+H2O H2CO3+OH-;
H2CO3+OH-;
(3)②①③ ;? 6×10-10mol・L-1
本题解析:(1)铵根离子水解,溶液呈酸性,c(H+)>c(OH-),.1mol?L-1的(NH4)2SO4溶液中,铵根离子水解微弱,所以得到溶液中的离子浓度大小为:c(NH4+)>c(SO42-)>c(H+)>c(OH-)。
(2)在NaHCO3溶液中存在碳酸氢根离子的水解平衡为:HCO3+H2O H2CO3+OH-,电离平衡为:HCO3-
H2CO3+OH-,电离平衡为:HCO3- H++CO32-;水的电离平衡,H2O
H++CO32-;水的电离平衡,H2O H++OH-。
H++OH-。
(3)Ksp=1.8×10-10mol2?L-2=C(Ag+)?C(Cl-),通过计算分别得到:①100mL蒸馏水中含银离子浓度和氯离子浓度相同;②100mL 0.2mol?L-1AgNO3溶液中Ag+浓度为0.2mol/l抑制沉淀溶解平衡,氯离子浓度=1.8×10-10÷0.2=9×10-10mol/L;③100mL 0.1mol?L-1氯化铝溶液中氯离子浓度为0.3mol/L,银离子浓度=6×10-10mol/L;④100mL 0.1mol?L-1盐酸溶液中氯离子浓度为0.1mol/L,银离子为1.8×10-9mol/L;综上所述大小顺序为:②①④③;②中氯离子的浓度9×10-10 mol/L;,③中银离子的浓度:6.0×10-10mol/L。
点评:本题考查了盐类水解的应用,溶液中离子浓度大小的比较,溶液中平衡的分析,溶液配制,溶度积的计算应用。
本题难度:一般
2、选择题 I2在KI溶液中存在下列平衡:I2(aq) + I一(aq)  I3一(aq)。测得不同温度下该反应的平衡常数值如下表:
I3一(aq)。测得不同温度下该反应的平衡常数值如下表:
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1100 | 841 | 680 | 533 | 409 |
 I3-(aq)的△H>0
I3-(aq)的△H>0 参考答案:B
本题解析:略
本题难度:一般
3、填空题 工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g) 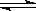 ?CH3OH(g)
?CH3OH(g)
(1)不同温度下的平衡转化率与压强的关系如图所示。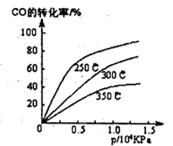
①该反应△H?0,△S?0(填“>”或“<”),则该反??自发进行(填“一定能”、“一定不能”、“不一定”)实际生产条件控制在250℃、l.3×l04kPa左右,选择此压强的理由是?。
(2)某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)="0.l" mol・L -1。
①该反应的平衡常数K=?:
②在其他条件不变的情况下,将容器体积压缩到原来的1/2,与原平衡相比,下列有关说法正确的是?(填序号)。
A.氢气的浓度减少
B.正反应速率加快,逆反应速率也加快
C.甲醇的物质的量增加
D.重新平衡时n(H2)/n(CH3OH)增大
③若保持同一反应温度将起始物质改为a mol CO、b mol H2、c mol CH30H,欲使平衡混合物中各组成与原平衡相同,则a、b应满足的关系为?,且欲使开始时该反应向逆反应方向进行,c的取值范围是?。
参考答案:(1)①<?<)?不一定?②该压强下,CO转化率已较高(90%左右),再增大压强CO转化率提高不大,且生产成本增加?(2)① 6.25?② b c?③ b = 2+2a? 1.8<c ≤2
本题解析:(1)①由图可知:在压强不变的情况下:升高温度,CO的转化率降低,说明升高温度,化学平衡向逆反应方向移动。逆反应方向是吸热反应。正反应是放热反应。所以ΔH<0.在温度不变时,增大压强,CO的转化率增大。说明增大压强化学平衡向正反应方向移动。ΔS<0..由于正反应是一个体系混乱程度减小的放热反应,所以无法确定该反应能否自发进行。②选择此压强的理由是在该压强下,CO转化率已较高(90%左右),再增大压强,CO转化率虽然提高但提高不大,且生产成本增加的多,效益反而降低。(2)①反应开始时CO H2CH3OH的浓度分别是1mo/L? 3mol/L 0mol/L,在反应过程中转化浓度分别是0.9mol/L 1.8mol/L 0.9mol/L.所以它们的平衡浓度分别是0.1mol/L 1.2mol/L 0.9mol/L所以达到化学平衡时平衡常数是K=(0.9)÷{0.1×(1.2)2}=" 6.25" ②将容器体积压缩到原来的1/2,化学平衡向正反应方向移动。与原平衡相比,正反应速率加快,逆反应速率也加快;各物质的浓度都增大,甲醇的物质的量也增加增加 ;? D.重新平衡时n(H2)/n(CH3OH)减小。正确选项为:bc.③若保持同一反应温度将起始物质改为a mol CO、b mol H2、c mol CH30H,欲使平衡混合物中各组成与原平衡相同,则a、b应满足的关系为b=2+2a.假如物质时由CH3OH转化生成,则开始时n(CH3OH)=2mol,因为平衡时n(CH3OH)=0.9mol/L×2L=1.8mol.所以欲使开始时该反应向逆反应方向进行,c的取值范围是 1.8<c ≤2
本题难度:困难
4、填空题 在某温度下,体积恒定的密闭容器中加入2 molN2和4 molH2,发生如下反应:
N2(g)+3H2(g) 2NH3(g);ΔH=―92.4 kJ/mol。达到平衡时,放出热量46.2 kJ。求:
2NH3(g);ΔH=―92.4 kJ/mol。达到平衡时,放出热量46.2 kJ。求:
(1)达到平衡时,N2的转化率为_______________, NH3的体积分数为?。
(2)若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均为正数,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同。a、b、c取值必须满足的一般条件是?,??。
(3)科学家发明了使NH3直接用于燃料电池的方法,其装置用铂黑作电极、加入电解质溶液中,一个电极通入空气,另一电极通入NH3。其电池总反应式为:4NH3+3O2=2N2+6H2O,电解质溶液应显 (填“酸性” 、“中性” 或“碱性” ),写出正极的电极反应方程式 。
参考答案:(1)25%? 20%?
(2)a+c/2="2,b+3c/2=4"
(3)碱性? O2+2H2O+4e-=4OH-
本题解析:(1)根据化学方程式可知消耗了0.5mol的氮气,所以氮气的转化率为25%,氨气的体积分数为1/(1.5+2.5+1)=20%;
(2)等效平衡;
(3)氨气溶于水容易与酸性溶液或中性溶液中的氢离子发生化学反应。
本题难度:一般
5、填空题 在一固定容积的密闭容器中,保持一定条件进行以下反应:X(气)+2Y(气) 3Z(气) ,已知加
3Z(气) ,已知加
2molX和3molY达到平衡后,生成amolZ。
(1)在相同实验条件下,若在同一容器中改为加入4molX和6molY,达到平衡后,Z的物质的量为______
mol。
(2)在相同实验条件下,若在同一容器中改为加入3molX和2molY,若要求在反应混合气体中Z体积分数不变,则还需加入Z__________mol。
(3)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加_________molY,_________mol Z,才能使平衡时Z为0.6amol。
参考答案:(1)2a?
(2)15
(3)0.4;2.1
本题解析:
本题难度:一般