时间:2019-05-30 05:07:19
1、选择题 下列物质属于同位素的一组是( )
A.O2与O5
B.淀粉和纤维素
C.1H和2H
D.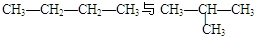
2、选择题 X、Y、Z、M是4种短周期元素,其中X、Y位于同一主族,Y与M,X与Z位于同一周期。X原子最外层电子数是其电子层数的3倍。Z原子的核外电子数比X原子少1。M是同周期中半径最大的元素(除稀有气体元素),下列说法正确的是
[? ]
3、填空题 下列原子序数所对应的元素组中,两者可形成离子键的是
[? ]
A.1和17
B.12和9
C.14和6
D.15和8
4、实验题 (5分)现有X、Y、Z三种元素,已知有如下情况:
①X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③ XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。
④ 两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白作用。
请完成下列问题:
(1)写出XZ和X2Y的化学式:XZ X2Y
(2)Z的单质溶于X2Y后,溶液起漂白作用的物质是 (写化学式)。
(3)写出X的单质在Z的单质中燃烧的化学方程式 。
(4)Z的单质能否与氢氧化钠溶液发生反应: (填“能”或“否”),若能,请写出反应的化学方程式: ? 。
(若不能反应,则此空不必填写)。
5、推断题 今有原子序数依次增大的A、B、C、D、E、F六种元素。已知A、C、F三原子的最外层共有11 个电子,这三种元素的最高价氧化物的水化物之间两两皆能反应且均生成盐和水。D和E各有如 下表所示的电子层结构。在一般情况下,B元素的单质不能与A、C、D、E元素的单质化合。 
按要求填空:
(1)各元素的元素符号分别为C____。E__,D和E两者的氢化物稳定性较强的是___(填化学式)。
(2)工业上制取单质D的化学方程式为___。
(3)A与C两元素的最高价氧化物对应的水化物反应的离子方程式为___。
(4)E与F形成E的最高价化合物,0.25 mol该固体物质与足量水充分反应,最终生成两种酸,并放出akJ的热量。写出该反应的热化学方程式:___。