ʱ��:2019-05-30 04:32:42
1��ѡ���� ��һ���¶��½�1mol CO��9molˮ���������ܱյ������з������з�Ӧ��
CO(g)+H2O(g)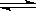 CO2(g)+H2(g)�ﵽƽ�����֪�÷�Ӧƽ�ⳣ��ΪK=1.0���ﵽ�µ�ƽ���CO2��H2�����ʵ���֮��Ϊ��?��
CO2(g)+H2(g)�ﵽƽ�����֪�÷�Ӧƽ�ⳣ��ΪK=1.0���ﵽ�µ�ƽ���CO2��H2�����ʵ���֮��Ϊ��?��
A��1.2mol
B��1.5mol
C��1.8mol
D��2.5mol
�ο��𰸣�C
���������������淴Ӧ���йؼ��㣬һ���������ʽ��
CO(g)+H2O(g)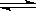 CO2(g)+H2(g)
CO2(g)+H2(g)
��ʼ����mol��? 1? 9? 0? 0
ת������mol)? x? x? x? x
ƽ������mol��? 1��x? 9��x? x? x
������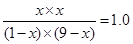
���x��9/10
����CO2��H2�����ʵ���֮��Ϊx��x��1.8mol����ѡC��
�����Ѷȣ�һ��
2��ѡ���� �ϳɰ���Ӧ��ƽ��״̬��ָ��������е�
A�����������������백���ɵ�����֮��Ϊ3��2
B���������ʱ�����������ܶȲ��ٸı�
C�����������������백����������֮��Ϊ1��2
D�����������ʵ�����������
�ο��𰸣�C
���������A.����ʱ�����������������백���ɵ�����֮�ȶ���3��2��Ӧ��Ϊ���������������백����������֮��Ϊ3��2ʱ��Ϊƽ��״̬��B.���������غ㣬�����������һֱ���䣬����ֲ��䣬���Բ�����û�дﵽƽ��״̬�����������ܶ�һֱ�����䡣D. ���������ʵ�������һֱ������
�����Ѷȣ�һ��
3������� ���ܱ������У���2.0molCO��10molH2O��ϼ��ȵ�800�棬�ﵽ����ƽ�⣺CO��g��+H2O��g��
�ο��𰸣��١����淴ӦCO��g��+H2O��g������
���������
�����Ѷȣ�һ��
4��ѡ���� ������ʵ��������������ԭ�����͵���
A����ˮ��������ƽ��Br2+H2O HBr+HBrO����������������Һ����Һ��ɫ��dz
HBr+HBrO����������������Һ����Һ��ɫ��dz
B���ϳɰ���Ӧ��Ϊ��߰��IJ��ʣ�������Ӧ��ȡ�����¶ȵĴ�ʩ
C����ӦCO(g)+NO2(g) CO2(g)+NO(g)(����ӦΪ���ȷ�Ӧ)����ƽ��������¶���ϵ��ɫ����
CO2(g)+NO(g)(����ӦΪ���ȷ�Ӧ)����ƽ��������¶���ϵ��ɫ����
D������2HI(g) H2(g)+I2(g)����ƽ�����С���������ʹ��ϵ��ɫ����
H2(g)+I2(g)����ƽ�����С���������ʹ��ϵ��ɫ����
�ο��𰸣�D
���������A����ˮ�д�������ƽ��Br2+H2O HBr+HBrO��������AgNO3��Һʱ��Br�C��Ag+��Ӧ������AgBr������ƽ�������ƶ���Br2Ũ�ȼ�С����Һ��ɫ��dz��������������ԭ�����ͣ�B���ϳɰ���ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ������IJ�����ߣ�������������ԭ�����ͣ�C�����ڷ�ӦCO(g)+NO2(g)
HBr+HBrO��������AgNO3��Һʱ��Br�C��Ag+��Ӧ������AgBr������ƽ�������ƶ���Br2Ũ�ȼ�С����Һ��ɫ��dz��������������ԭ�����ͣ�B���ϳɰ���ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ������IJ�����ߣ�������������ԭ�����ͣ�C�����ڷ�ӦCO(g)+NO2(g) CO2(g)+NO(g)Ϊ���ȷ�Ӧ�����������¶ȣ�ƽ�������ƶ���NO2Ũ��������ϵ��ɫ���������������ԭ�����ͣ�D�����ڷ�Ӧ2HI(g)
CO2(g)+NO(g)Ϊ���ȷ�Ӧ�����������¶ȣ�ƽ�������ƶ���NO2Ũ��������ϵ��ɫ���������������ԭ�����ͣ�D�����ڷ�Ӧ2HI(g) H2(g)+I2(g)���������������ķ�Ӧ����С���������ƽ�ⲻ�ƶ�����ɫ�������������СʹI2Ũ����������ģ���������������ԭ�����͡�
H2(g)+I2(g)���������������ķ�Ӧ����С���������ƽ�ⲻ�ƶ�����ɫ�������������СʹI2Ũ����������ģ���������������ԭ�����͡�
�����Ѷȣ�һ��
5������� (10��) �ݻ��̶����ܱ������У��������淴Ӧ��M(g)+N(g)  ?2P(g)+Q(g) ��H��0��
?2P(g)+Q(g) ��H��0��
��ش��������⣺
(1����ij�¶��£���Ӧ�����ʼŨ�ȷֱ�Ϊ��c(M)��1 mol��L-1,c(N)��2.4 mol��L-1���ﵽƽ���M��ת����Ϊ60������ʱN ��Ũ����?��P ���������Ϊ_________��
(2������Ӧ�¶����ߣ�M��ת����____________ (�������С�����䡱����ͬ����ƽ����Է�������____________����������ܶ�____________��
�ο��𰸣���1��1.8 mol��L-1?30%
��2������?��С?����
�����������
�����Ѷȣ���