时间:2019-05-30 03:30:38
1、选择题 下列叙述不正确的是
A.在稀盐酸中 c(H+)=c(Cl—)+c(OH—)
B.常温下,在0.1mol/L的HNO3溶液中由水电离出的c(H+)<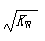
C.将Na2CO3水溶液加热、蒸干,最后得到NaOH固体
D.酸与碱完全中和,所得溶液的pH可能大于7
参考答案:C
本题解析:A、根据电荷守恒,稀盐酸中c(H+)=c(Cl—)+c(OH—)成立,正确;B、硝酸的存在对水的电离起抑制作用,所以水电离出的c(H+)<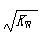 ,正确;C、盐的水解是吸热反应,加热促进水解,但第二步
,正确;C、盐的水解是吸热反应,加热促进水解,但第二步
水解非常微弱,所以不会有二氧化碳气体放出,平衡不会一直正向移动,因此最终得到的仍是碳酸钠固体,错误;D、酸与碱完全中和,所得溶液的pH大于7、小于7、等于7都有可能,依据酸、碱的强弱决定,正确,答案选C。
本题难度:一般
2、选择题 下列分散系中存在溶质的电离平衡的是
A 硝酸溶液? B 氢氧化钙溶液? C硫酸钡悬浊液? D 氢氧化铜悬浊液
参考答案:D
本题解析:弱电解质存在电离平衡。氢氧化铜为弱碱,属于弱电解质。
本题难度:一般
3、选择题 若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是(?)
A.生成了一种强酸弱碱盐
B.弱酸溶液和强碱溶液反应
C.强酸溶液和弱碱溶液反应
D.一元强酸溶液和一元强碱溶液反应
参考答案:B
本题解析:若pH=3的酸溶液c(H+)=10-3mol/L; pH=11的碱溶液,c(OH-)=10-3mol/L;二者等体积混合后溶液呈酸性,可能是酸是弱酸,碱是强碱,当H+与OH-中和后,未电离的酸分子又电离产生了H+。使溶液显酸性。因此正确选项为B。
本题难度:一般
4、填空题 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA物质的量 浓度(mol·L-1) | NaOH物质的量 浓度(mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | C1 | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
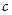 (A-)与
(A-)与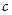 (Na+)的大小关系是 。
(Na+)的大小关系是 。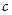
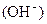 = mol·L-1。
= mol·L-1。 参考答案:(每小题3分)(1)> (2)C (3)弱 Na+>A->OH->H+ (4)10-5
本题解析:(1)若HA是弱酸,则恰好反应后是强碱弱酸溶液,呈碱性。(2)、根据电荷守恒有:c(Na+)+c(OH-)=c(H+)+c(A-) ,pH=7时,c(OH-)=c(H+),所以c(Na+)= c(A-)。
(3)丙组中HA酸过量,但溶液显碱性,所以HA是弱酸。
(4)因溶液pH=9,c(OH-)=10-6mol/L,全部来源于水的电离。
本题难度:一般
5、选择题 下述根据下列操作和现象,所得结论正确的是
| | 实验操作及现象 | 实验结论 |
| A | 分别向2mL0.1mol·L-1CH3COOH溶液和2mL0.1mol·L-1H3BO3溶液中滴加等浓度的NaHCO3溶液,前者有气泡产生,后者无明显现象 | 酸性:CH3COOH>H2CO3>H3BO3 |
| B | 向浓度均为0.1mol·L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液,产生黄色沉淀 | 溶度积:Ksp(AgCl)<Ksp(AgI) |
| C | 向无水乙醇中加入浓H2SO4,加热,产生的气体通入酸性KMnO4溶液,紫色褪去 | 证明生成了乙烯 |
| D | 将少量的溴水滴入NaI溶液中,再滴加CCl4,振荡、静置,溶液分为两层:上层溶液无色,下层溶液紫红色 | 氧化性:Br2>I2 |
参考答案:AD
本题解析:A、根据复分解反应的规律:强酸制弱酸的原理,醋酸与碳酸氢钠溶液反应生成二氧化碳,说明醋酸酸性大于碳酸,而H3BO3与碳酸氢钠溶液混合,无气体产生,说明酸性H2CO3>H3BO3,正确;B、向浓度均为0.1mol·L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液,产生黄色沉淀,说明AgI比AgCl更难溶,则Ksp(AgCl)>Ksp(AgI),错误;C、向无水乙醇中加入浓H2SO4,加热,产生的气体通入酸性KMnO4溶液,紫色褪去,不能说明生成了乙烯,因为乙醇易挥发,且乙醇也能使酸性高锰酸钾溶液褪色,错误;D、将少量的溴水滴入NaI溶液中,则生成碘单质和NaBr,再滴加CCl4,碘在四氯化碳中的溶解度大于在水中的溶解度,且四氯化碳的密度大于水与水不互溶,在下层,所以振荡、静置,溶液分为两层:上层溶液无色,下层溶液紫红色,正确,答案选AD。
考点:考查反应的原理判断,现象与结论的分析正误判断的知识。
本题难度:困难
|