ʱ��:2019-05-30 03:09:16
1������� ij�¶��µ���Һ�У�c(H+)=1��0��10X c(OH-)=1��0��10Y��X��Y�Ĺ�ϵ����ͼ��ʾ��
��1�����¶��£�������Һ��pHΪ____________ ��
��2�����¶��£�0��01mol/LNaOH��Һ��pHΪ_____________ ��
��3�����¶��£�0��005mol/L������Һ��pHΪ_____________________ ��
��4�����¶��£�pH=4��������Һ��pH=10��NaOH��Һ��һ�������ϣ���Ϻ�ǡ�÷�Ӧ������ǰ������Һ��NaOH��Һ�����Ϊ________________________ ��
2��ѡ���� 25��ʱ����ϡ��ˮ��μ���ϡ�����У�����Һ��pH=7ʱ�����й�ϵ����ȷ���ǣ�������
A��c��NH4+��=c��Cl-��
B��c��H+��=c��OH-��
C��c��NH4+����c��Cl-��
D��c��OH-��+c��Cl-��=c��H+��+��NH4+��
3��ѡ���� ��֪�¶�Tʱˮ�����ӻ�����ΪKW�����¶��£���Ũ��Ϊamol?L-1��һԪ��HA��bmol?L-1һԪ��BOH�������ϣ����ж�����Һ�����Ե������ǣ�������
A��a=b
B�������Һ��pH=7
C�������Һ�У�c��H+��=
| Kw |
4��ѡ���� 25��ʱ����20mL?0.1mol/L NaOH��Һ����μ���0.2mol/L������Һ��������ͼ��ʾ��
�й�����Ũ�ȹ�ϵ�ıȽ��У�����ȷ���ǣ�������
A����A�㣺c��Na+����c��OH-����c��CH3COO-����c��H+��
B����B�㣺c��OH-���Tc��H+����c��Na+���Tc��CH3COO-��
C����C�㣺c��CH3COO-����c��Na+����c��H+����c��OH-��
D����C�㣺c��CH3COO-��+c��CH3COOH���T2c��Na+��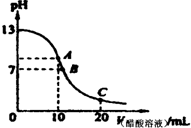
5��ѡ���� �����£���pH=11��ij����Һ��pH=3��ij����Һ�������ϣ�����˵����ȷ���ǣ�������
A����������Һ�����ԣ������ɵ���һ��Ϊǿ��ǿ����
B�������õ���Һ�ʼ��ԣ������������ǿ��������
C����������Һ�����ԣ��������ǿ����������Һ��Ӧ
D����������Һ��pH=5���������ǿ����������Һ��Ӧ