时间:2019-05-30 02:53:25
1、选择题 下列有关计算的分析正确的是
A.某溶液100mL,其中含硫酸0.03mol,硝酸0.04mol,若在该溶液中投入1.92 g铜粉微热,反应后放出一氧化氮气体约为0.015mol
B.室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧.则a、b的关系是a=4b+c
C.已知某温度Ksp(Ag2S)=6×10-50,Ksp(AgCl)=2×10-6,则2AgCl(s)+S2-(aq) Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×10-37
Ag2S(s)+2Cl-(aq)的平衡常数约为6.7×10-37
D.在25 ℃下,将2a mol・L-1的氨水与0.02 mol・L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),则用含a的代数式表示NH3・H2O的电离常数 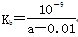
参考答案:D
本题解析:A.某溶液100mL,其中含硫酸0.03mol,硝酸0.04mol,则氢离子物质的量是0.1mol。若在该溶液中投入1.92 g铜粉即0.03mol铜微热,根据方程式8H++3Cu+2NO3-=3Cu2++4H2O+2NO↑可知反应中硝酸根和氢离子过量,则反应后放出一氧化氮气体约为0.02mol,A错误;B.室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不能支持燃烧,这说明剩余气体是NO,则根据方程式4NO2+O2+2H2O=4HNO3、3NO2+H2O=HNO3+2NO可知4b+1.5c=a,B错误;C.已知某温度Ksp(Ag2S)=6×10-50,Ksp(AgCl)=2×10-6,则2AgCl(s)+S2-(aq) Ag2S(s)+2Cl-(aq)的平衡常数=
Ag2S(s)+2Cl-(aq)的平衡常数=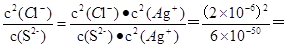 6.7×1037,C错误;D.在25 ℃下,将2a mol・L-1的氨水与0.02 mol・L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),则根据电荷守恒可知溶液显中性,溶液中c(NH4+)=c(Cl-)=0.01mol/L,一水合氨的浓度是amol/L―0.01mol/L,因此用含a的代数式表示NH3・H2O的电离常数
6.7×1037,C错误;D.在25 ℃下,将2a mol・L-1的氨水与0.02 mol・L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),则根据电荷守恒可知溶液显中性,溶液中c(NH4+)=c(Cl-)=0.01mol/L,一水合氨的浓度是amol/L―0.01mol/L,因此用含a的代数式表示NH3・H2O的电离常数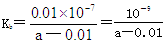 ,D正确,答案选D。
,D正确,答案选D。
考点:考查化学反应计算
本题难度:困难
2、简答题 在含有酚酞的0.1mol/L氨水中加入少量的NH4Cl晶体,则溶液颜色( )
A.变蓝色
B.变深
C.变浅
D.不变
参考答案:因氨水电离生成氢氧根离子,则酚酞遇碱变红,当加入少量的NH4Cl晶体后,NH4+离子浓度增大,根据同离子效应,加入NH4Cl后,氨水的电离平衡向逆方向移动,抑制氨水电离,从而c(OH-)变小,颜色变浅.
故选:C.
本题解析:
本题难度:一般
3、选择题 对于碳酸溶液中的电离平衡,电离常数的表达式中正确的是
[? ]
A.K=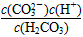
B.K=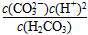
C.K1=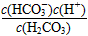
D.K2=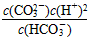
参考答案:C
本题解析:
本题难度:简单
4、选择题 pH相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌全部溶解且放出气体一样多,则下列说法正确的是
A.反应开始时的速率:甲=乙
B.反应所需时间:甲<乙
C.反应开始时,酸的物质的量浓度:甲=乙
D.反应结束时,溶液pH:甲<乙
参考答案:A
本题解析:A.pH相同的盐酸(甲)和醋酸(乙),两种溶液中氢离子浓度相等,所以开始反应速率相等,A正确;B.反应过程中,醋酸电离导致醋酸中氢离子浓度减少速率小于盐酸中氢离子浓度减少速率,盐酸中的氢离子浓度小于醋酸中氢离子浓度,盐酸反应速率小于醋酸,所以反应所需时间:甲>乙,B错误;C.pH相同的盐酸(甲)和醋酸(乙),醋酸是弱电解质,氯化氢是强电解质,所以C(HCl)<C(CH3COOH),C错误;D.若最后锌粒全部溶解且放出气体一样多,可能是盐酸恰好反应而醋酸过量,也可能是盐酸和醋酸都过量,如果盐酸恰好反应而醋酸过量,则反应后溶液的pH甲>乙,如果盐酸和醋酸都过量,要根据氢离子浓度确定溶液的pH大小,D错误;选A。
考点:考查化学反应速率的大小比较。
本题难度:一般
5、填空题 已知HA是一种弱酸。请回答下列问题:
(1)现有一种含有HA和其钠盐NaA的溶液。
①组成该溶液的微观粒子有?;
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是?;
③若向该溶液中逐滴加入NaOH溶液时,下列图像能表示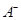 离子数目变化趋势的是?(填字母)。
离子数目变化趋势的是?(填字母)。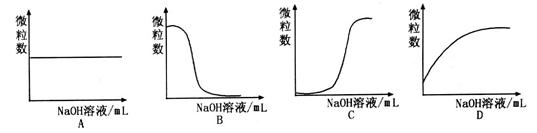
(2)现将1体积0.04mol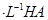 溶液和1体积0.02mol
溶液和1体积0.02mol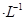 NaOH溶液混合,得到2体积混合溶液。
NaOH溶液混合,得到2体积混合溶液。
①若该混合液显碱性,则其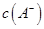 ?0.01 mol
?0.01 mol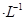 (填“<”、“=”或“>”);
(填“<”、“=”或“>”);
②若该混合液显酸性,则溶液中所有离子的浓度由大到小的顺序是?。
参考答案:(1)①H2O、HA、H+、Na+、OH?、A-(2分,有错不得分)
②A-+H+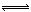 HA(2分,不写可逆号也可)
HA(2分,不写可逆号也可)
③D(1分)
(2)①<(1分)
②c(A-)>c(Na+)>c(H+)>c(OH?)(2分)
本题解析:(1)①溶液中的微观粒子既包括离子,也包括分子,所以含有HA和其钠盐NaA的溶液的微观粒子有:H2O、HA、H+、Na+、OH?、A-
②加入少量盐酸,HCl与NaA反应生成HA,所以离子方程式为:A-+H+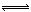 HA
HA
③溶液含有HA和NaA,逐滴加入NaOH溶液,HA与NaOH反应生成NaA和H2O,所以A2-数目逐渐增大,故D项正确。
(2)①1体积0.04mol/LHA溶液和1体积0.02mol/LNaOH溶液混合,HA过量,得到等量的NaA和HA,若该混合液显碱性,则c(H+)<c(OH?),根据电荷守恒c(H+)+c(Na+)=c(OH?)+c(A-)可得c(A-)<0.01mol?L?1。
②若该混合液显酸性,则HA的电离程度大于NaA的水解程度,溶液中所有离子的浓度由大到小的顺序是:c(A-)>c(Na+)>c(H+)>c(OH?)
本题难度:一般