时间:2019-05-30 02:45:46
1、填空题 将锌片和铜片以下图所示两种方式分别插入同浓度稀硫酸中。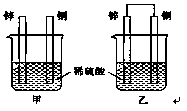
(1)以下叙述中,正确的是?(填标号)。
A.装置甲、乙中铜片表面均无气泡产生
B.装置甲、乙中稀硫酸的浓度均减小
C.装置乙中锌片是正极,铜片是负极
D.装置乙中产生气泡的速率比装置甲快
(2)装置乙中,总反应的离子方程式为 ?;若导线上通过0.2 mol电子,消耗锌的质量为 ?g。
2、填空题 按要求完成下列原电池电极反应式或总反应的化学方程式。
(1)负极(Fe)?;正极(石墨)?
电解质溶液(稀硫酸)总反应?
(2)负极(Cu)?; 正极(石墨)?
电解质溶液(FeCl3溶液)总反应?
(3)用Fe和Cu作电极材料,以浓HNO3为电解质溶液构成的原电池,则负极的电极反应式为?;总反应为?
3、选择题 如图所示原电池装置中,电解质溶液为硫酸,下列有关叙述错误的是
A.锌做负极发生氧化反应
B.供电时的总反应为:Zn + H+ = Zn2+ + H?2
C.该装置可实现化学能转化为电能
D.产生1molH2,消耗锌的质量32.5g
4、选择题 2011年7月19日,美国能源部西北太平洋国家实验室的科学家和来自中国武汉大学访问学者组成的研究小组合作开发钠离子充电电池,研究人员采用廉价的钠离子同时使用纳米氧化锰和锂材料作电极制作出了钠离子充电电池,其工作示意图如下。关于该电池说法中正确的是
[? ]
A.放电时A极作正极?
B.放电时Na+向负极移动
C.充电时是将化学能转化为电能?
D.充电时阳极反应为:Li-e-=Li+
5、填空题 Ⅰ.如图所示,在大试管里放入一段光亮无锈的弯成螺旋状的铁丝,把试管倒插入水中,把这个装置这样放置约一周后,观察到铁丝发生的变化是______________________,原因是____________________.试管里的水面会上升,最终上升高度约为_______,原因是_________________________________________________________________________________________________________________.
Ⅱ.A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
(1)A中反应的离子方程式为__________________________________________.
(2)B中Sn电极的电极反应式为________________________________________,Sn电极附近溶液的pH__________(填“增大”、“减小”或“不变”).
(3)C中被腐蚀的金属是________,总反应式为________________________.比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是______________________.