时间:2018-03-17 06:58:10
1、选择题 下列叙述中,正确的是( )
A.IA族元素,其原子半径越大金属性越弱
B.核外电子排布相同的两种微粒,化学性质一定相同
C.氨基酸具有两性,则多肽及由多肽形成的蛋白质均具有两性
D.苯分子具有不饱和性,苯与乙炔一样都可使酸性高锰酸钾溶液褪色
参考答案:A.IA族元素,从上到下原子半径逐渐增大,金属性逐渐增强,故A错误;
B.核外电子排布相同的两种微粒,化学性质不一定相同,如F-和Na+,二者性质不同,故B错误;
C.氨基酸、多肽以及蛋白质中含有氨基和羧基,既能和酸反应,又能与碱反应,故C正确;
D.苯性质较稳定,不能使酸性高锰酸钾溶液褪色,故D错误.
故选C.
本题解析:
本题难度:简单
2、推断题 有五种短周期元素xA、yB、zC、mD、nE,其中x+y+z+m+n=57。已知A元素的气态氢化物与其最高价氧化物对应的水化物在常温下能化合成一种化合物;C元素的原子最外层电子数是其电子层数的3倍;D元素的最高正化合价与最低负化合价的绝对值相等,且D与C只能形成一种化合物;E单质在空气中燃烧能生成一种淡黄色固体。试回答:
(1)A元素名称__________,它在元素周期表中的位置___________ 。B元素原子的电子式___________,E元素简单离子的电子排布式是___________。
(2)分别写出A和B的最高价氧化物对应水化物的分子式________、_________
(3)写出C和D形成的化合物的化学式__________,其中心原子轨道的杂化方式是___________。
(4)写出A的气态氢化物的结构式_________,其分子的空间构型为_________,属于___________分子。
参考答案:(1)氮;第二周期VA族;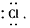 ;1s22s22p6
;1s22s22p6
(2)HNO3;HClO4
(3)SiO2;sp3
(4)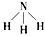 ;三角锥形;极性
;三角锥形;极性
本题解析:
本题难度:一般
3、选择题 超重元素“稳定岛”的假设预言:自然界中可能存在着原子序数为114的元素的稳定同位素208X.1999年人们发现了114号元素,有力地支持了“稳定岛”学说.请你根据已知的元素周期律预测208X在元素周期表中的位置
A.第八周期Ⅷ族
B.第七周期ⅥA族
C.第七周期ⅣA族
D.第六周期ⅠB族
参考答案:C
本题解析:根据已有的元素周期律,第七周期如果排满,应排到118号,即118号元素应位于第七周期0族(第18列),由此可知114号元素应位于同一周期,第ⅣA族(第14列).
本题难度:一般
4、选择题 下列说法正确的是( )
A.第ⅤA族元素都是非金属元素
B.磷比氮难以与氢化合生成气态氢化物
C.气态氢化物的稳定性:PH3>NH3>H2O
D.酸性:HNO3>H3PO4>H2SO4
参考答案:A.第ⅤA族元素含有Sb、Bi等金属元素,故A错误;
B.非金属性N>P,元素的非金属性越强,越易与氢气反应,且氢化物的稳定性越强,故B正确;
C.非金属性O>N>P,元素的非金属性越强,氢化物的稳定性越强,应为PH3<NH3<H2O,故C错误;
D.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,应为HNO3>H2SO4>H3PO4,故D错误.
故选B.
本题解析:
本题难度:简单
5、选择题 位于同一周期的五种短周期元素A、B、C、D、E它们的原子序数依次增大,已知A、B为金属,其余为非金属。A、B原子序数之和数值上等于A元素的原子量;C、D的最外层电子数均为偶数;电解熔融的化合物BE2是工业上生产单质B的方法。下列叙述正确的是
[? ]
A.A的氧化物的熔点大于B的氧化物
B.C既能与强酸溶液也能与强碱溶液反应
C.D、E的单质均能与氧气直接化合生成其最高价氧化物
D.含A、E元素的某物质具有漂白作用
参考答案:D
本题解析:
本题难度:一般