ʱ��:2018-03-17 06:25:28
1��ѡ���� ����ʱ�����й��ڵ������Һ��������ȷ����?��?��
A��ϡ��pH=10�İ�ˮ����Һ���������ӵ�Ũ�Ⱦ�����
B����ͬ�������ͬŨ�ȵ������������Һ���ֱ���ͬŨ�ȵ�����������Һǡ����ȫ��Ӧʱ���������ĵ�����������Һ�����
C��pH=11��NaOH��Һ��pH=11�İ�ˮ�ֱ�ϡ��100�����pHǰ��һ��С�ں���
D���ֱ��к�pH���������ͬ������ʹ��ᣬ���������������Ƶ����ʵ�����
�ο��𰸣�C
���������A ������ˮϡ����Һ����������������Ũ�ȶ����ͣ���ˮϡ�Ͱ�ˮ��c(H��)����
B ���������������ʵ�����ȣ�����NaOH�����ʵ���Ҳ��ȣ���������NaOH�������ͬ
C ��NaOH��ǿ�ϡ��100����PH=9����ˮ��������ڵ���ƽ��,��ˮϡ�ͣ�ƽ�����ƣ�c(OH��)Ӧ����NaOH��Һ�е�c(OH��)��pH>9
D ��pH���������ͬ������ʹ��ᣬ���������������Ƶ����ʵ�����
�����Ѷȣ���
2��ѡ���� ������Һ�и�����Ũ�ȹ�ϵ����ȷ���ǣ�������
A��0.1mol/LCH3COOH��Һ�У�c��CH3COO-��+c��CH3COOH��=0.1mol/L
B��NaHCO3��Һ�У�c��H+��+c��Na+��=2c��CO32-��+c��HCO3-��+��OH-��
C��CH3COONa��Һ�У�c��Na+����c��CH3COO-������OH-����c��H+��
D��Na2S��Һ�У�2c��Na+��=c��S2-��+c��HS-��+c��H2S��
�ο��𰸣�A��CH3COOH��Һ�и��ݴ�����غ��֪��c��CH3COO-��+c��CH3COOH��=0.1mol/L����A��ȷ��
B��NaHCO3��Һ���Ե��ԣ����������Ӵ���������������������Ӵ��ĸ������������c��H+��+c��Na+��=2c��CO32-��+
c��HCO3-��+��OH-������B��ȷ��
C��CH3COONa��Һ�У�CH3COONa�TCH3COO-+Na+������������ˮ���Լ��ԣ���c��Na+����c��CH3COO-������OH-����c��H+����ˮ��ij̶Ȳ�����c��CH3COO-������OH-������C��ȷ��
D��Na2S��Һ��n��Na��=2n��S�����������غ��֪��12c��Na+��=c��S2-��+c��HS-��+c��H2S������D����
��ѡD��
���������
�����Ѷȣ�һ��
3��ѡ���� �����ж�ij��(HA)��ǿ����ʵ���ʵ��(����)
A��������������ڲ��ֽ�
B��0.01 mol��L��1�����pH��2
C����������ܽ�Cu(OH) 2
D��������CaCO3��Ӧ�ų�CO2
�ο��𰸣�B
���������ǿ�������ȫ���룬�����ڵ���ƽ�⣬B��������Ũ�Ⱥ�һԪ���Ũ����ȣ�˵����ȫ���룬�����ڵ���ƽ�⣬����ѡ��B��ȷ��A������ȶ��ԣ�C��D���DZ������ԣ�������ȷ���Ƿ���ǿ����ʣ���ѡB��
������������ʵ�֤�����ǻ�����ǿ����ʶԱȽ��еġ����������ǿ����������������������ʴ��ڵ���ƽ�⣬��ǿ����ʲ����ڵ���ƽ�⡣���ֻҪ֤���е���ƽ����ڣ���֤����������ʡ�
�����Ѷȣ���
4��ѡ���� 25��ʱ���й�����ĵ���ƽ�ⳣ�����£������й�˵����ȷ���ǣ�������
| ���ữѧʽ | CH3COOH | HCN | H2CO3 ����ƽ�ⳣ����25�棩 1.8��10-5 4.9��10-10 K1=4.3��10-7K2=5.6��10-11 |
�ο��𰸣�A�����ݵ���ƽ�ⳣ����֪����ǿ��˳��Ϊ��CH3COOH��HCN��HCO3-������Խ������Ӧ�������������ˮ��̶�Խ����Һ��PHԽ�����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��
pH��Na2CO3����pH��NaCN����pH��CH3COONa������A����
B����c��Na+����c��CN-����������Һ�����Կ�֪c��H+����c��OH-������Һ�ʼ��ԣ�a��b��a�Tb�����ϣ���B����
C������������������ʣ���ˮ�ٽ����룬����������μ�ˮ����Һ�ĵ�������������С��pH�ȼ�С��������ĵ���̶�������C����
D��Na2CO3��NaHCO3�����ʵ��������Һ�У����ڵ���������Na+��H+����������OH-��HCO3-��CO32-��������Һ�����ԣ�����C��Na+��+c��H+��=c��OH-��+c��HCO3-��+2c��CO32-������D��ȷ��
��ѡD��
���������
�����Ѷȣ���
5��ѡ���� pH��2��A��B��������Һ��lmL���ֱ��ˮϡ�͵�1000mL������Һ��pH����Һ���(V)�Ĺ�ϵ��ͼ��ʾ��������˵����ȷ����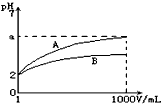
[? ]
A��A��B��������Һ���ʵ���Ũ��һ�����
B��ϡ�ͺ�A����Һ�����Ա�B����Һǿ
C��a��5ʱ��A��ǿ�ᣬB������
D����A��B�������ᣬ��5��a>2
�ο��𰸣�C
���������
�����Ѷȣ�һ��