时间:2018-03-17 06:14:56
1、选择题 有甲、乙两瓶醋酸稀溶液,测得甲的pH=a,乙的pH=a+1.下列推断正确的是?(?)
A.物质的量浓度c(甲)是c(乙)的10倍
B.溶液中的c(OH-)甲是乙的10倍
C.由水电离产生的c(H+)乙是甲的10倍
D.与等量的NaOH反应消耗甲、乙两酸的体积V(乙)>10V(甲)
参考答案:CD
本题解析:醋酸是弱电解质,不能全部电离,所以,A错;.溶液中的c(OH-)乙是甲的10倍,B错;C正确,根据水的电离平衡常数可知由水电离产生的c(H+)乙是甲的10倍;D正确,若醋酸是强酸,则与等量的NaOH反应消耗甲、乙两酸的体积V(乙)=10V(甲),而实际上醋酸是弱酸,且酸性越强,电离程度越低;
本题难度:简单
2、选择题 将0.1mol?L-1的醋酸钠溶液20mL与0.1mol?L-1的盐酸10mL混合后,溶液显酸性,则溶液中有关微粒的浓度关系正确的是( )
A.c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH)
B.c(CH3COO-)>c(H+)>c(CH3COOH)>c(Cl-)
C.c(CH3COO-)=c(Cl-)>c(H+)>c(CH3COOH)
D.c(Na+)+c(H+)=c(CH3COO-)+c(Cl-)+c(OH-)
参考答案:将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后,反应后NaAc和HAc的物质的量相等,溶液显酸性,说明HAc电离程度大于Ac-水解程度,
A.HAc为弱电解质,部分电离,应有c(HAc)>c(H+),故A错误;
B.反应后NaAc和HAc的物质的量相等,溶液显酸性,说明HAc电离程度大于Ac-水解程度,则(Ac-)>c (Cl-),HAc为弱电解质,部分电离,应有c(HAc)>c(H+),故B错误.
C.反应后NaAc和HAc的物质的量相等,溶液显酸性,说明HAc电离程度大于Ac-水解程度,则(Ac-)>c (Cl-),故C错误;
D.溶液遵循电中性原则,应有c(Na+)+c(H+)=c(Ac-)+c(Cl-)+c(OH-),故D正确.
故选D.
本题解析:
本题难度:简单
3、选择题 对于0.1 mol/L的醋酸溶液,下列说法正确的是?
A.加水稀释后,溶液中c(H+)和c(OH-)都减少
B.温度升高后,溶液的pH增大
C.加入少量Na2CO3固体,醋酸电离平衡向左移动
D.加入少量冰醋酸后,溶液的c(H+)增大
参考答案:D
本题解析:醋酸是弱酸,学生促进电离,氢离子浓度降低,c(OH-)增大,A不正确;升高温度,促进电离,氢离子浓度增大,pH降低,B不正确;C中碳酸钠能结合氢离子,降低氢离子浓度,促进醋酸的电离,C不正确;D中增大醋酸的浓度,溶液的酸性增强,氢离子浓度增大,D正确,所以答案选D。
点评:该题是中等难度试题的考查,也是高考中的常见题型和考点。该题的关键是明确醋酸的电离平衡特点,然后结合题意灵活运用勒夏特列原理即可,难度不大。
本题难度:一般
4、填空题 I,已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸K =1.75×10-5
碳酸K1=4. 30×10-7 K2=5.61×10-11
亚硫酸K1=1.54×10-2 K2=1.02×10-2
(1)写出碳酸的第一级电离平衡常数的表达式:K1=___。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:____>____>___ 。
(3)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是___(填序号)。
A.c(CH3COO -)
B.c(H+)
C.醋酸电离平衡常数
D.醋酸的电离程度
Ⅱ,某化工,一废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01 mol.L-1。排放前拟用沉淀法除去这两种离子,查找有关数据如下:
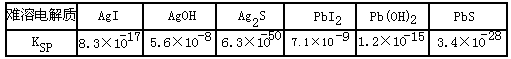
参考答案:(1)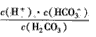
(2)H2CO3 ;HSO3- ;HCO3-
(3)AD
(4)B
(5)9×10 -9 mol . L-1
本题解析:
本题难度:一般
5、选择题 有a、b、c、d四种一元酸的溶液,实验表明:
①物质的量浓度相同的a、c溶液中,分别滴入甲基橙试液后,a溶液呈黄色而c溶液呈橙色;②物质的量浓度相同的b、c的钠盐溶液相比较,b的钠盐溶液pH小于c的钠盐溶液pH;③a酸跟d的盐反应生成a的盐和d酸.由此可以确定四种酸的酸性由强到弱的顺序正确的是
A.b?a?c?d
B.d?a?c?b
C. b?c?a?d
D.c?d 91eXAm.org?a?b
参考答案:C
本题解析:略
本题难度:一般