时间:2017-11-11 02:25:07
1、选择题 pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000mL,其pH值与溶液体积的关系如图,下列说法正确的是 
[?]
A.A、B两种酸溶液的物质的量浓度一定相等
B.若1< a < 4,则A、B都是弱酸
C.稀释后,A酸溶液的酸性比B酸溶液强
D.若a = 4,则A是弱酸,B是强酸。
参考答案:B
本题解析:
本题难度:一般
2、选择题 关于强弱电解质的叙述正确的是:(?)
A.强电解质都是离子化合物,弱电解质都是共价化合物
B.强电解质都是可溶性化合物,弱电解质都是难溶性化合物
C.弱电解质的水溶液的导电能力比强电解质溶液弱
D.强电解质的稀溶液中无溶质分子,弱电解质的溶液中存在溶质分子
参考答案:D
本题解析:A.强电解质不一定是离子化合物,如盐酸是共价化合物,但它在水溶液中能完全电离,它是强电解质,弱电解质也不一定是共价化合物,如氢氧化铝是弱电解质,但它是离子化合物.A错误;B.强弱电解质和溶于水的电解质是否完全电离有关,与是否难易溶于水无关.硫酸钡难溶于水,但它是强电解质,乙酸易溶于水,但它是弱酸.故B错误;C.溶液导电能力取决于溶液中离子浓度的大小,与电解质强弱无关,强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强,C错误;D.强电解质在水中没有达到饱和前全电离,所以强电解质的稀溶液中无溶质分子,弱电解质部分电离层,弱电解质的溶液中存在溶质分子,D正确;选D。
本题难度:一般
3、选择题 在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65g大小相同的锌粒,则下列各图比较符合客观事实的是( )
A.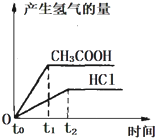
B.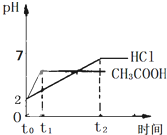
C.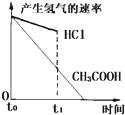
D.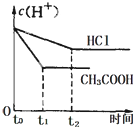
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列说法正确的是(?)
A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
C.在高锰酸钾溶液中,H+、K+、SO42-、葡萄糖分子可以大量共存
D.已知:Ksp(AgCl)=1.8×10-10, Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2CrO4的溶解度小于AgCl
参考答案:A
本题解析: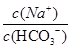 =
=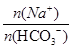 ,NaHCO3溶液加水稀释时,n(Na+)保持不变,n(HCO3-)减小,所以c(Na+)/c(HCO3-)的比值保持增大,A选项正确;根据物料守恒,浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:3c(Na+)=2[c(CO32-)+c(HCO3-)],B选项错误;高锰酸钾会氧化葡萄糖,C选项错误;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即x═
,NaHCO3溶液加水稀释时,n(Na+)保持不变,n(HCO3-)减小,所以c(Na+)/c(HCO3-)的比值保持增大,A选项正确;根据物料守恒,浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:3c(Na+)=2[c(CO32-)+c(HCO3-)],B选项错误;高锰酸钾会氧化葡萄糖,C选项错误;假设Ag2CrO4饱和溶液中Ag+的浓度为x,则CrO42-的浓度为0.5x,由溶度积常数的表达式可知Ksp(Ag2CrO4)=x2×0.5x=0.5x3=2.0×10-12,x3=4.0×10-12,即x═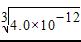 ,因为AgCl饱和溶液中Ag+的浓度为
,因为AgCl饱和溶液中Ag+的浓度为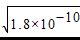 ,所以的溶解度大于AgCl,D选项错误。
,所以的溶解度大于AgCl,D选项错误。
本题难度:一般
5、选择题 常温下,体积相等,pH值都是3的盐酸和醋酸,分别加水稀释到pH等于4,然后用0.01mol/L的烧碱溶液将酸中和,下列说法中正确的是(?)
A.稀释前盐酸和醋酸的物质量浓度相等
B.稀释后醋酸溶液的体积与盐酸溶液的体积相等
C.中和醋酸所用烧碱溶液的体积较大
D.完全中和后两种溶液的pH值仍然相等
参考答案:C
本题解析:略
本题难度:简单