时间:2017-11-11 01:42:30
1、填空题 (附加题2)(2分)天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。其氧化镍样品组成为Ni0.97O,试计算该晶体中Ni2+与Ni3+的离子数之比。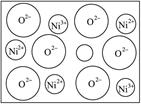
参考答案:6∶91
本题解析:设1 mol Ni0.97O中含Ni3+x mol,Ni2+(0.97-x) mol;根据电中性:3x mol+2(0.97-x)
mol="2×1" mol x="0.06" Ni2+为(0.97-x) mol="0.91" mol,离子数之比Ni3+∶Ni2+=0.06∶0.91=6∶91。
本题难度:简单
2、选择题 下列分子的空间构型为V型的是(? )
A.H2O
B.NH3
C.HF
D.CH4
参考答案:A
本题解析:
本题难度:简单
3、填空题 (12分)有A、B、C、D、E、F六种元素,已知:它们位于三个不同的短周期,核电荷数依次增大;A与E、B与F分别同主族;A、E分别都能与D按原子个数1∶1或2∶1形成化合物;B、C分别能与D按原子个数1∶1或1∶2形成化合物。
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学
式?、?。
(2)右图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示?。E与D按原子个数比1∶1形成的化合物的电子式为?。
(3)人们通常把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
| 化学键 | F―D | F―F | B―B | F―B | B==D | D==D |
| 键能/ kJ・mol?1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
参考答案:(1)NaHCO3、CH3COONa(或其他有机酸钠盐)?(2)氢键;过氧化钠的电子式
(3)① a>c>b?② Si(s) + O2(g) ="=" SiO2(s);△H= ?990.7kJ・mol?1
本题解析:略
本题难度:一般
4、选择题 氮化硼是一种新合成的结构材料,它是一种超硬、耐磨、耐高温的物质。下列各组物质熔化时所克服的微粒间的作用力类型与氮化硼熔化所克服的微粒间的作用力类型都相同的是
A.氯化钠和金刚石
B.金刚石和二氧化硅
C.冰和干冰
D.二氧化硫和二氧化硅
参考答案:B
本题解析:
解析:氮化硼熔化时克服的是共价键。A选项中,氯化钠和金刚石熔化时分别克服的是离子键和共价键,不一致;C选项中,冰和干冰熔化时分别克服的是氢键和分子间作用力;D选项中,二氧化硫和二氧化硅熔化时分别克服的是分子间作用力和共价键,故不正确;所以选B项。
本题难度:一般
5、选择题 下列说法错误的是( )
A.分子晶体、原子晶体、离子晶体都不导电
B.一般规律熔点:分子晶体<离子晶体<原子晶体
C.构成晶体的原子之间都有化学键
D.晶体中只要有阴离子就有阳离子
参考答案:C
本题解析:A、正确,没有可以自由移动的带电粒子;B、正确;D、正确,是离子晶体;稀有气体分子中不存在化学键,所以C不正确,其余都是正确的,答案选C。
本题难度:一般