时间:2017-11-05 22:58:39
1、填空题 下列物质?①Cu?②液态SO2?③纯醋酸?④NaHCO3?⑤Ba(OH)2溶液
I.属于非电解质的是______;(填序号)
Ⅱ.(1)NaHCO3是一种______(填“强”或“弱”)电解质;
(2)写出HCO3-水解的离子方程式:______;
(3)常温下,0.1mol-L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH?-五种微粒的浓度由大到小的顺序为:______.
Ⅲ.Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液.
(1)该Ba(OH)2溶液的物质的量浓度为______;
(2)溶液中由水电离出c(OH?-)=______;
(3)与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=______.
Ⅳ.醋酸是一种弱电解质.?某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如右图所示.则图______(填“I”或“Ⅱ”)为醋酸稀释的图象.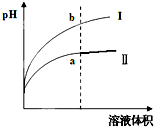
参考答案:Ⅰ、①Cu是金属单质能导电,但单质即不是电解质也不是非电解质;
②液态SO2是共价化合物不能导电,不是电解质,属于非电解质;
③纯醋酸溶于水能导电,是电解质;
④NaHCO3是离子化合物,是电解质;
⑤Ba(OH)2溶液是混合物,即不是电解质也不是非电解质.
故选:②;
Ⅱ、(1)NaHCO3属于盐,在水溶液中完全电离,属于强电解质,故答案为:强;
(2)HCO3-水解生成碳酸与氢氧根离子,水解离子方程式为HCO3-+H2O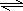
H2CO3+OH-,故答案为:HCO3-+H2O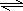
H2CO3+OH-;
(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,c(OH-)>c(H+),说明HCO3-水解程度大于其电离程度,故c(Na+)>c(HCO3-)、c(H2CO3)>c(CO32-),水解程度不大所以c(HCO3-)>c(H2CO3)、c(HCO3-)>c(OH-),溶液中氢氧根来源于水的电离与HCO3-水解,故c(OH-)>c(H2CO3),所以c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-),
故答案为:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-);
Ⅲ、(1)pH=13的Ba(OH)2溶液中c(OH-)=0.1mol/L,根据氢氧根守恒可知,溶液中c[Ba(OH)2]=12c(OH-)=0.5×0.1mol/L=0.05mol/L,故答案为:0.05mol/L;
(2)pH=13的Ba(OH)2溶液中氢离子使由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH?-),故水电离出c(OH?-)=c(H+)=10-13mol/L,
故答案为:10-13mol/L;
(3)pH=13的Ba(OH)2溶液中c(OH-)=0.1mol/L,与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,假定体积分别为1L、9L,所得溶液pH=11,即混合后溶液中c(OH?-)=10-3mol/L,令盐酸的浓度为amol/L,则混合后溶液中n(OH?-)=1L×0.1mol/L-9L×amol/L=10-3mol/L×(1L+9L),解得a=0.01,
故答案为:0.01mol/L;
Ⅳ、盐酸是强电解质,醋酸是弱电解质,相同pH值的盐酸和醋酸溶液分别加水稀释,醋酸稀释促进醋酸电离继续产生氢离子,故稀释相同的倍数,醋酸的PH增大的较小,故图Ⅱ为醋酸稀释的图象,故答案为:Ⅱ.
本题解析:
本题难度:一般
2、选择题 向NaOH(aq)滴入HAc(aq)的过程中,溶液中离子浓度的大小可能正确的是
A.c(OH-) = c(Na+) > c(Ac-) > c(H+)
B.c(Na+) > c(OH-) = c(Ac-) > c(H+)
C.c(Na+) > c(Ac-) > c(OH-) > c(H+)
D.c(H+) > c(Ac-) > c(Na+) > c(OH-)
参考答案:BC
本题解析:A.根据电荷守恒,溶液中存在,c(OH-)+c(Ac-)=c(Na+)+c(H+),如c(OH-)=c(Na+),应存在c(Ac-)=c(H+),故A错误;B.如为NaOH和NaAc的混合物,溶液呈碱性,可满足c(Na+)>c(OH-)=c(Ac-)>c(H+),故B正确;C.当溶液为NaAc时,溶液呈碱性,可满足c(Na+)>c(Ac-)>c(OH-)>c(H+),故C正确;
D.阳离子大于阴离子,电荷不是守恒,故D错误.故选BC。
考点:本题考查离子浓度大小比较,题目难度不大,注意电荷守恒的运用,把握盐类水解和盐类水解的原理。
本题难度:一般
3、选择题 常温下,盐酸与氨水混合,所得溶液pH=7,则此溶液中
A.c(NH4+)<c(Cl-)
B.c(NH4+)=c(Cl-)
C.c(NH4+)>c(Cl-)
D.无法确定c(NH4+)与c(Cl-)的关系
参考答案:B
本题解析:根据溶液的电中性可知c(NH4+)+c(H+)=c(Cl-)+c(OH-),由于溶液pH=7,即c(H+)=c(OH-),所以c(NH4+)=c(Cl-),答案选B。
考点:考查溶液中离子浓度大小比较
点评:在判断离子浓度大小时,应该利用好电荷守、物料守恒和质子守恒等基本定律。
本题难度:简单
4、选择题 属于正确的水解反应离子方程式的是( ? )
A.S2-+2H2O?H2S+2OH-
B.CH3COOH+H2O?CH3COO-+H3O+
C.NH4++H2O?NH3?H2O+H+
D.CH3COOH+OH-?CH3COO-+H2O
参考答案:C
本题解析:
本题难度:一般
5、填空题 (10分)(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,原因是(用离子方程式表示): ;
(2)氯化铝水溶液呈 性,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表
示): ;
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)已知MgCl2·6H2O晶体在空气中加热时,释放部分结晶水,同时生成Mg(OH)Cl(碱式氯化镁)或生成MgO。下列是关于MgCl2·6H2O的综合应用:
请回答下列问题:
①在上图的括号内应填的是在_______________环境中加热。
②Mg(OH)2固体存在如下溶解平衡:Mg(OH)2(固)  Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
Mg2++2OH-。向体系中加入(请填出两种不同类别的物质)_____________________________________________________ 有利于Mg(OH)2溶解。
③已知AnBm的离子积=c (Am+) n ·c (Bn-) m,式中c (Am+) n和c (Bn-) m表示离子的物质的量浓度,在室温时若测得Mg(OH)2饱和溶液的pH值为11,其离子积为___________________。
参考答案:(1)酸, Ag++ H2O 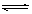 AgOH + H+
AgOH + H+
(2)酸, Al3++3H2O 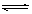 Al(OH)3+3H+, Al2O3 ;
Al(OH)3+3H+, Al2O3 ;
(3) ①HCl气流 ②酸、水、酸性气体、饱和NH4Cl等(任选两种)(每空1分)
③5×10-10(2分)
本题解析:(1)AgNO3是强酸弱碱盐,水解显酸性。
(2)氯化铝也是强酸弱碱盐,水解显酸性。铝离子水解生成氢氧化铝和氯化氢,水解吸热,加热促进水解。同时氯化氢的挥发,进一步促进水解,所以最终得到的是氢氧化铝,灼烧得到氧化铝。
(3)氯化镁水解显酸性,所以要得到氯化镁晶体,在加热时需要防止水解,因此在硫化氢的气流中加热即可。根据氢氧化镁的溶解平衡可知,要促进溶解,就必须使平衡向正反应方向移动。所以可以通过消耗OH-或镁离子来实现。根据离子积常数的概念可知,离子积常数是电离出的离子的浓度的幂之积,Mg(OH)2饱和溶液的pH值为11,则OH-的浓度为10-3mol/L,则镁离子浓度为5×10-4mol/L,所以氢氧化镁的离子积常数为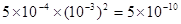 。
。
本题难度:困难