时间:2017-11-05 22:43:36
1、选择题 若以w1和w2分别表示浓度为c1mol/L和c2mol/L硫酸的质量分数,已知2 w1=w2,则下列推断正确的是(硫酸的密度比纯水的大)
A.2c1=c2
B.2c2=c1
C.c2>2c1
D.c1<c2<2c1
2、填空题 (9分)在常温下,下列五种溶液:
①0.1mol/L NH4Cl?②0.1mol/L CH3COONH4?③0.1mol/L NH4HSO4
④0.1mol/L NH3·H2O和0.1mol/L NH4Cl混合液?⑤0.1mol/L NH3·H2O
请根据要求填写下列空白:
(1)溶液①呈??性(填“酸”、“碱”或“中”),其原因是?用离子方程式表示)
(2)在上述五种溶液中,pH最小的是?;c(NH4+)最小的是??﹝填序号﹞
(3)比较溶液②、③中c(NH4+)的大小关系是②?③﹝填“>”、“<”或“=”)
(4)在溶液④中,?离子的浓度为0.1mol/L;NH3·H2O和?离子的物质的量浓度之和为0.2 mol/L
(5)常温下,测得溶液②的pH=7,则说明CH3COO-的水解程度________(填“>”、“<”或“=”) NH4+的水解程度,CH3COO-与NH4+浓度的大小关系是:c(CH3COO-) ???c(NH4+)(填“>”、“<”或“=”)
3、选择题 未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且有些可以再生。下列属于新能源的是
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥燃料电池 ⑦风能 ⑧氢能
A.①②③④
B.⑤⑥⑦⑧
C.③④⑤⑥
D.除①②外
4、选择题 若a、b、c、d均大于零,下列能正确表示燃烧热的热化学方程式为
A.CH3CH2OH(l) + 3O2 (g) = 2CO2 (g) + 3H2O(l)ΔH =-a kJ/mol
B.CH4 (g) + 2O2 (g) = 2H2O(g) + CO2 (g)ΔH =-b kJ/mol
C.H2 (g) +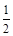 O2 (g) = H2O(l)ΔH = c kJ/mol
O2 (g) = H2O(l)ΔH = c kJ/mol
D.2CH≡CH(g) + 5O2(g) =4CO2 (g) + 2H2O(l)ΔH =-d kJ/mol
5、填空题 (4分)某工厂甲、乙两车间,分别排放的污水中含有大量的Ag+、Ba2+、Fe3+、Na+、Cl-、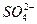 、
、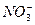 、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则
、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则
(1)甲车间污水中含有的四种离子可能是___________________________。
(2)乙车间污水中含有的四种离子可能是___________________________。