ʱ��:2017-11-05 22:43:36
1��ѡ���� ����w1��w2�ֱ��ʾŨ��Ϊc1mol/L��c2mol/L�����������������֪2 w1��w2���������ƶ���ȷ���ǣ�������ܶȱȴ�ˮ�Ĵ�
A��2c1��c2
B��2c2��c1
C��c2��2c1
D��c1<c2<2c1
�ο��𰸣�C
��������������ʵ�����Ũ��Ϊc1 mol?L-1���ܶ�Ϊ��1�����ʵ�����Ũ��Ϊc2mol?L-1������Һ���ܶ�Ϊ��2����
c1= 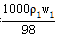 ��c2=
��c2= 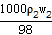 ��
��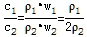 ����Ũ������ܶȴ���ˮ����Һ��Ũ��Խ���ܶ�Խ�����1����2��
����Ũ������ܶȴ���ˮ����Һ��Ũ��Խ���ܶ�Խ�����1����2��
��c2��2c1��
��ѡC��
���������⿼�����ʵ���Ũ�������������ļ�����Ƚϣ���Ŀ�Ѷ��еȣ�ע��Ũ������ܶȴ���ˮ����Һ��Ũ��Խ���ܶ�Խ��
�����Ѷȣ���
2������� ��9�֣��ڳ����£�����������Һ��
��0.1mol/L NH4Cl?��0.1mol/L CH3COONH4?��0.1mol/L NH4HSO4
��0.1mol/L NH3��H2O��0.1mol/L NH4Cl���Һ?��0.1mol/L NH3��H2O
�����Ҫ����д���пհף�
��1����Һ�ٳ�??�ԣ���ᡱ��������С�������ԭ����?�����ӷ���ʽ��ʾ��
��2��������������Һ�У�pH��С����?��c(NH4+)��С����??�z����ũ{
��3���Ƚ���Һ�ڡ�����c(NH4+)�Ĵ�С��ϵ�Ǣ�?�۩z�������������������
��4������Һ���У�?���ӵ�Ũ��Ϊ0.1mol/L��NH3��H2O��?���ӵ����ʵ���Ũ��֮��Ϊ0.2 mol/L
��5�������£������Һ�ڵ�pH=7����˵��CH3COO����ˮ��̶�________��������������������� NH4+��ˮ��̶ȣ�CH3COO����NH4+Ũ�ȵĴ�С��ϵ�ǣ�c(CH3COO��) ???c��NH4+)���������������������
�ο��𰸣���1����? NH4+ + H2O 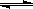 ?NH3��H2O + H+?��2���ۣ���?��?
?NH3��H2O + H+?��2���ۣ���?��?
��3��<?��4��Cl��?��NH4+?(5)? = �� =
�����������
�����Ѷȣ�һ��
3��ѡ���� δ������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ�������Ⱦ������Щ����������������������Դ����
����Ȼ�� ��ú �ۺ��� ��ʯ�� ��̫���� ��ȼ�ϵ�� �߷��� ������
A���٢ڢۢ�
B���ݢޢߢ�
C���ۢܢݢ�
D�����٢���
�ο��𰸣�B
�������������Դ���ص�����Դ�ḻ����ʹ��ʱ�Ի�������Ⱦ�������Ⱦ������Щ����������������Щ���������жϣ�ʯ�͡���Ȼ����ú���ڻ�ʯ��Դ����ʱ���ڲ����γɣ��Dz���������Դ��̫���ܡ�ȼ�ϵ�ء����ܡ������������Դ�ҿ���������������Դ�ķ���ѡB��
���㣺��������Դ���жϡ�
�����Ѷȣ���
4��ѡ���� ��a��b��c��d�������㣬��������ȷ��ʾȼ���ȵ��Ȼ�ѧ����ʽΪ
A��CH3CH2OH(l) + 3O2 (g) = 2CO2 (g) + 3H2O(l)��H =��a kJ/mol
B��CH4 (g) + 2O2 (g) = 2H2O(g) + CO2 (g)��H =��b kJ/mol
C��H2 (g) +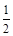 O2 (g) = H2O(l)��H = c kJ/mol
O2 (g) = H2O(l)��H = c kJ/mol
D��2CH��CH(g) + 5O2(g) =4CO2 (g) + 2H2O(l)��H =��d kJ/mol
�ο��𰸣�A
���������ȼ������ָ��һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų�������������A��ȷ��B��Ӧ����Һ̬ˮ��C�С�HӦС��0��D����Ȳ�Ļ�ѧ������Ӧ��1mol����ѡA��
�����Ѷȣ�һ��
5������� ��4�֣�ij�����ס��������䣬�ֱ��ŷŵ���ˮ�к��д�����Ag+��Ba2+��Fe3+��Na+��Cl-��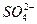 ��
��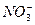 ��OH-�е����֡������Ե����ŷŻ���ɽϴ���Ⱦ�������Ϻ����ŷţ��������Ⱦ�̶ȡ��ֲ�ü׳����ŷŵ���ˮ�ʼ��ԡ���
��OH-�е����֡������Ե����ŷŻ���ɽϴ���Ⱦ�������Ϻ����ŷţ��������Ⱦ�̶ȡ��ֲ�ü׳����ŷŵ���ˮ�ʼ��ԡ���
��1���׳�����ˮ�к��е��������ӿ�����___________________________��
��2���ҳ�����ˮ�к��е��������ӿ�����___________________________��
�ο��𰸣���1��OH-��Cl-��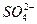 ��Na+
��Na+
��2��Ag+��Ba2+��Fe3+��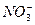
������������������ܷ��������ͼ׳����ŷŵ���ˮ�ʼ��Կ����жϳ��׳�����ˮ���ҳ�����ˮ�зֱ�����Щ���ӡ�
�����Ѷȣ���