时间:2017-11-05 22:20:49
1、选择题 在冶金工业上,均不能用通常化学还原剂制得的金属组是( )
A.Na、Mg、Al
B.Na、K、Zn
C.Fe、Cu、Ag
D.Na、Ca、Cu
2、选择题 下列关于金属冶炼的说法正确的是( ? )
A.金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定
B.Cu的湿法冶炼是将金属钠投入到CuSO4溶液中,从而置换出铜
C.Fe通常采用热还原法冶炼,加入石灰石的目的是除去过量的碳
D.由于Al的活泼性强,故工业上采用电解熔融AlCl3的方法生产Al
3、简答题 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.
若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁:
①a电极材料为______,其电极反应式为______.
②电解液d可以是______(填编号)
A.纯水?B.NaCl?溶液?C.NaOH溶液?D.CuCl2溶液
③液体c为苯,其作用是______;在加入苯之前,对d溶液进行加热处理的目的是______.
④为了在短时间内看到白色沉淀,可以采取的措施是______.
A.改用稀硫酸做电解液?B.适当增大电源电压
C.适当缩小两电极间距离?D.适当降低电解液温度.
4、选择题 下图中A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,C为盛有稀硫酸的电解槽,e、f为Pt电极。接通电源后,发现d点显红色。下列有关说法正确的是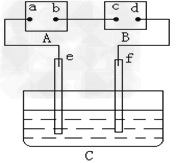
[? ]
A.电源A上的a极是正极
B.d极上的电极反应方程式为2Cl--2e-=Cl2↑
C.e、f极上产生的气体体积比为2:1
D.C中溶液的pH增大
5、简答题 合理、高效利用金属矿物,将其中的金属从其化合物中还原出来用于生产和制造各种金属材料,这一过程在工业上称为金属的冶炼.
(1)以HgO为原料冶炼Hg,冶炼方法是______.
(2)铝热法是冶炼金属的方法之一,写出铝热法炼铁(Fe2O3)的化学方程式:______.引发铝热反应的实验操作是:______.
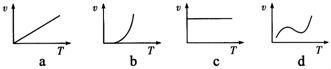
(3)某些金属氧化物粉末和铝粉在一定条件下可以发生铝热反应.下列反应速率(υ)和温度(T)的关系示意图中与铝热反应最接近的是:______(填字母).