时间:2017-11-05 22:11:27
1、选择题 在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是(?)
CO2(g)+H2(g)。CO2的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是(?)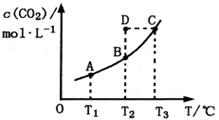
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的ΔH>0
CO2(g)+H2(g)的ΔH>0
B.在T2时,若反应处于状态D,则一定有v正<v逆
C.平衡状态A与C相比,平衡状态A的c(CO)小
D.恒压密闭容器中通入1mol CO(g)和1mol H2O(g),发生上述反应,当反应达到平衡后,在其他条件不变时,再通入1mol H2O(g)和1mol CO(g)的混合气体,v正、v逆反应速率随时间t变化的示意图如下。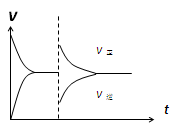
2、填空题 (8分)(1)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)  CO2(g)+H2(g),该反应是放热反应
CO2(g)+H2(g),该反应是放热反应
CO和H2O浓度变化如左下图,则0~4min的平均反应速率v(CO)=______mol/(L・min) 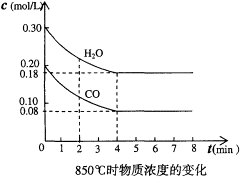
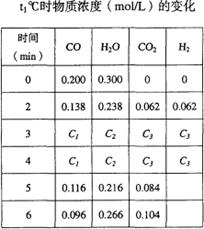
(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。
①表中3min~4min之间反应处于_________状态;C1数值________0.08mol/L(填大于、小于或等于)。
②反应在4min~5min问,平衡向逆方向移动,可能的原因是________(单选),
表中5min―6min之间数值发生变化,可能的原因是________(单选)。
A.增加水蒸气
B.降低温度
C.使用催化剂
D.增加氢气浓度
3、选择题 500℃条件下,在恒容密闭容器中,充入1molNO2存在如下平衡2NO2(g) N2O4(g)?,平衡后,向容器内再充入1molNO2,下列说法正确的
N2O4(g)?,平衡后,向容器内再充入1molNO2,下列说法正确的
A.平衡向正反应方向移动
B.平衡常数K增大
C.NO2的转化率变小
D.容器内气体颜色先变深后变浅,最后比原来还要浅
4、选择题 以下事实不能用勒夏特列原理解释的是(? )
A.增大压强,有利于二氧化硫和氧气反应生成三氧化硫
B.工业制取硫酸和合成氨反应都要使用催化剂
C.合成氨工业生产中,把合成塔中的氨气不断抽出
D.实验室常用排饱和食盐水的方法收集氯气
5、选择题 如图所示,向A、B中均充入1molX、l rnol Y,起始时A、B的体积都等于aL。在相同温度、外界压强和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:
X(g)+Y(g) 2Z(g)+W(g) △H<0,达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g)+W(g) △H<0,达平衡时,A的体积为1.4aL。下列说法错误的是
[? ]
A.反应速率:v(B)>v(A)
B.A容器中x的转化率为80%
C.平衡时的平均摩尔质量:
D.平衡时Y体积分数:A<B