时间:2017-11-05 20:54:49
1、选择题 下图所示各种装置中能构成原电池的是
A.①②③
B.④⑤⑥
C.①③⑤
D.②④⑥
参考答案:C
本题解析:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应。装置①③⑤具备这四个条件,为原电池;②中酒精是非电解质,不能构成原电池,④中没有形成闭合回路,不能构成原电池,;⑥中电极相同,不能构成原电池,故C项正确。
本题难度:一般
2、选择题 铜锌原电池(如图)工作时,下列叙述正确的是 ( )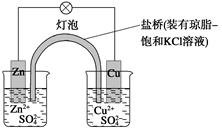
A.正极反应为:Zn-2e-===Zn2+
B.电池反应为:Zn+Cu2+===Zn2++Cu
C.在外电路中,电子从正极流向负极
D.盐桥中的K+移向ZnSO4溶液
参考答案:B
本题解析:A.Zn为活泼金属,作负极, 故Zn-2e-===Zn2+是负极反应式;B.电池反应为:Zn+Cu2+===Zn2++Cu,正确;C.在外电路中,电流从正极流向负极,电子从负极流向正极,原说法错误;D.根据溶液电荷守恒,盐桥中的K+移向消耗Cu2+的CuSO4溶液中,原说法不正确。
考点:盐桥电池的工作原理。
本题难度:一般
3、选择题 X、Y、Z三种金属,X、Y组成原电池,X是负极;把Y放在Z的硝酸盐溶液中,Y表面有Z析出。其活泼顺序是
[? ]
A.X>Y>Z
B.Z>Y>X
C.X>Z>Y
D.Y>X>Z
参考答案:A
本题解析:
本题难度:一般
4、选择题 某原电池的总反应方程式为:2Fe3+ +Cu=== 2Fe2+ + Cu2+,能实现该反应的为( )
| ? | A | B | C | D | |||||||||||||||||||||||||||||||||||||||||||
| 正极材料 | Cu | 石墨 | Fe | Ag | |||||||||||||||||||||||||||||||||||||||||||
| 负极材料 | Fe | Cu | Cu | Cu | |||||||||||||||||||||||||||||||||||||||||||
| 电解质液 | CuSO4 | Fe2(SO4)3 | FeCl3 | AgNO3 参考答案:B 本题解析:根据总的反应式可知,铜失去电子,铁离子得到电子,所以原电池中负极材料是铜,正极材料是比铜不活泼的金属或石墨等,而电解质溶液中必须含有铁离子,例如硫酸铁等,答案选B。 本题难度:一般 5、填空题 低碳经济呼唤新能源和清洁环保能源。煤化工中常需研究不同温度下的平衡常数、投料比及热值等问题。
(1)上述正反应方向是?反应(填“放热”或“吸热”)。 (2)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g)发生上述反应,CO和H2O(g)浓度变化如下图,则0~4 min的平均反应速率v(CO)=______ mol/(L・min)。 t1℃时物质浓度(mol/L)的变化 
①表中3 min~4 min之间反应处于_____状态;C1数值_____0.08 mol/L (填大于、小于或等于)。 ②反应在4 min~5 min,平衡向逆方向移动,可能的原因是____(单选),表中5 min~6 min之间数值发生变化,可能的原因是______(单选)。 A.增加水蒸气? B.降低温度? C.使用催化剂? D.增加氢气浓度 (4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为:?。 (5)若在850℃进行,设起始时CO和H2O(g)共为5mol,水蒸气的体积分数为X;平衡时CO转化率为Y,试推导Y随X变化的函数关系式为?。 (6) 工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等。已知: N2(g) + 2O2(g) =2NO2(g)?△H =" +67.7" kJ・mol-1 N2H4(g) + O2(g) =N2(g) + 2H2O(g)?△H = -534.0 kJ・mol-1 NO2(g)  1/2N2O4(g)?△H = -26.35 kJ・mol-1 1/2N2O4(g)?△H = -26.35 kJ・mol-1试写出气态联氨在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式: ________________________________________________________。 参考答案:(1)放热?(2分)(2)0.03 (2分)? 本题解析:(1)根据表中数据可知,随着温度的升高,平衡常数逐渐减小,说明升高温度,平衡向逆反应方向移动,因此正反应是放热反应。 本题难度:一般 |