时间:2017-09-25 19:19:49
1、填空题 氨是一种重要的化工原料,氨的合成与应用是当今重要研究内容之一。不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2起始物质的量之比为1∶3)。
 压强(Mpa) 压强(Mpa) 氨的平 氨的平衡含量(%) 温度(℃) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 9 5.4 5.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
| ? | 反应速率 | 平衡常数K | 氨的体积分数 |
| 变化情况 | ? | ? | ? |
参考答案:(1)(1分)放热。
(2)(2分)压强过大,需要的动力越大,对材料的强度和设备制造的要求也越高。
(3)(3分)
?
?
?
增大
减小
可能增大也可能减小
(4)(2分)C。
本题解析:略
本题难度:一般
2、选择题 化学与环境保护密切相关。下列叙述中正确的是
[? ]
A.处理废水时加入明矾可作为消毒剂以除去水中的杂质
B.垃圾是放错地方的资源,应分类回收利用
C.绿色化学的核心是应用化学原理对环境污染进行治理
D.为提高农作物的产量和质量,应大量使用化肥和农药
参考答案:B
本题解析:
本题难度:简单
3、填空题 (12分) 氮化硅硬度大、熔点高、不溶于酸(氢氟酸除外),是一种重要的结构陶瓷材料。一种用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅。一种合成氮化硅的工艺主要流程如下: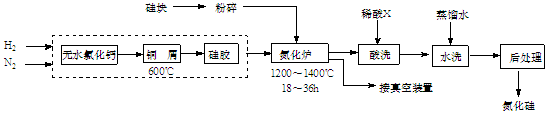
(1)净化N2和H2时,铜屑的作用是:?;硅胶的作用是?。
(2)在氮化炉中3SiO2(s)+2N2(g)=Si3N4(s) △H=-727.5kJ/mol,开始时为什么要严格控制氮气的流速以控制温度:?;体系中要通入适量的氢气是为了?。
(3)X可能是?(选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(4)用硅粉作硅源、叠氮化钠(NaN3)作氮源,直接燃烧生成氮化硅(发生置换反应),该反应的化学方程式为:?。
参考答案:(1)除去原料气中的氧气(2分);除去生成的水蒸气(2分)。
(2)这是放热反应,防止局部过热,导致硅熔化熔合成团,阻碍与N2的接触(2分);
将体系中的氧气转化为水蒸气,而易被除去(若答将整个体系中空气排尽也可得分)(2分)。
(3)硝酸(2分)?(4)9Si+4NaN3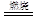 3Si3N4 +4Na↑(2分)
3Si3N4 +4Na↑(2分)
本题解析:(1)由于氧气和水蒸气都能腐蚀氮化硅,而氮气和氢气中含有水蒸气和氧气,所以铜屑的作用是除去氧气,硅胶是除去水蒸气的。
(2)因为这是放热反应,如果温度过高,局部过热,会导致硅熔化熔合成团,阻碍与N2的接触;通入氢气能将体系中的氧气转化为水蒸气,而易被除去。
(3)由于关于硅中含有铜的氧化物,在反应中氧化铜能被还原生成铜,因此要除去铜应该选择硝酸,盐酸和硫酸不能溶解铜,氢氟酸能腐蚀氮化硅。
(4)由于是置换反应,所以另一种生成物是钠,方程式未9Si+4NaN3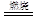 3Si3N4 +4Na↑。
3Si3N4 +4Na↑。
本题难度:一般
4、选择题 下列变化中,属于物理变化的是(? )
①石油的分馏 ②煤的干馏?③石油的裂化 ④铝热反应⑤由乙烯变为聚乙烯
⑥氧气转变为臭氧⑦乙烯催熟果实 ⑧苯遇溴水?⑨海水蒸馏法制取淡水
A.①②③④
B.①②⑤⑦
C.①⑧⑨
D.①②⑥⑨
参考答案:C
本题解析:有新物质生成的是化学变化,反之是物理变化。所以①⑧⑨是物理变化,其余都是化学变化,答案选C。
本题难度:简单
5、填空题 我国是氧化铝生产大国,工业上每生产1 t氧化铝将排出1~2 t赤泥,赤泥大量堆积会对环境造成严重污染。赤泥中主要成分及含量:CaO约占46%、SiO2约占22%、Al2O3约占7%、Fe2O3约占11%、TiO2约占5%及少量其他物质。
⑴一种利用废弃赤泥的方法是将赤泥配成一定的液固比,作为一种吸收剂,吸收热电厂排放的含SO2的烟气,写出吸收SO2时可能发生的化学反应方程式? ▲?。
⑵为综合利用赤泥中的各种成分,某科研小组设计了如下工艺流程:
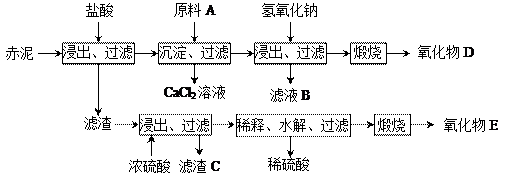 |
参考答案:⑴CaO+SO2=CaSO3?或Ca(OH)2+SO2=CaSO3+H2O
⑵①Fe2O3?C?
②OH-+Al(OH)3=AlO2-+2 H2O
③TiOSO4+2H2O=TiO(OH)2↓+H2SO4或TiOSO4+2H2O=TiO2・H2O↓+H2SO4
本题解析:略
本题难度:简单