时间:2017-09-25 19:14:58
1、填空题 铁及其化合物与生产、生活关系密切。
(1)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
①该电化腐蚀称为 。
②图中A和B区域相比较,腐蚀较慢的是 (填字母)。
(2)实验室经常用到FeCl3溶液,在配制FeCl3溶液时常需加入少量 的 ;将FeCl3溶液和碳酸氢钠溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为 。
(3)已知t℃时,反应FeO(s)+CO(g) Fe( s) +CO2(g)的平衡常数K= 0.25。
Fe( s) +CO2(g)的平衡常数K= 0.25。
①t℃时,反应达到平衡时n(CO2):n(CO)=
②若在1L密闭容器中加人0.02 mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时
FeO(s)转化率为50%,则x= 。
2、选择题 既可以发生消去反应,又能被氧化成醛的物质是( )
A.2-甲基-1-丁醇
B.2,2-二甲基-1-丁醇
C.2-甲基-2-丁醇
D.2,3-二甲基-2-丁醇
3、填空题 (10分)(1)同浓度的下列溶液:①NH4Al(SO4)2 ②NH4Cl ③CH3COONH4,其中c(NH4+) 由小到大的顺序是 (填序号,下同)。
(2)同浓度的下列溶液:①(NH4)2SO4 ②NH4Cl ③Na2CO3 ④NaHCO3,其中pH 由大到小的顺序是 。
(3)现有下列物质①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡固体⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KCl ⑧NaOH溶液 请用以上物质回答下列问题。
属于强电解质且在上述状态下能导电的是 ;
属于弱电解质的是 ;
属于非电解质,但溶于水后的水溶液能导电的是 。
4、选择题 把物质的量浓度均为0.1mol・L-1的HA和BOH溶液等体积混合,下列说法错误的是
A.若HA为弱酸,BOH为弱碱,则有C(H+)+C(B+)===C(OH-)+ C(A-)
B.若HA为强酸,BOH为弱碱,则有C(A-)>C(B+) >C(H+) >C(OH-)
C.若HA为弱酸,BOH为强碱,则有C(B+) >C(A-) >C(OH-) >C(H+)
D.若HA为强酸,BOH为强碱,则有C(H+)= C(A-)= C(B+)= C(OH-)=0.1mol・L-1
5、填空题 (7分)某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:
H2A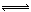 H++HA- HA-
H++HA- HA-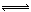 H++A2-
H++A2-
已知相同浓度时的电离程度α(H2A)> α(HA-),设有下列四种溶液:
(A)0.01mol.L-1的H2A溶液
(B)0.01mol.L-1的NaHA溶液
(C)0.01mol.L-1的HCl与0.04mol.L-1的NaHA溶液等体积混合液
(D)0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1) c(H+)最大的是
(2)在0.01mol.L-1的NaHA溶液中2C(A2- )+(C(HA-)+C C(OH-)-C(H+)=
(3) 0.02mol.L-1的NaOH与0.02 mol.L-1的NaHA溶液等体积混合显 性原因
(用离子方程式表示)