时间:2017-09-25 16:47:52
1、选择题 在0.1 mol/L的NH3・H2O溶液中,下列关系正确的是(?)
A.c(NH3・H2O)>c(OH-)>c(NH4+)>c(H+)
B.c(NH4+)>c(NH3・H2O)>c(OH-)>c(H+)
C.c(NH3・H2O)>c(NH4+)=c(OH-)>c(H+)
D.c(NH3・H2O)>c(NH4+)>c(H+)>c(OH-)
参考答案:A
本题解析:
【错解分析】电解质溶液中离子浓度大小比较问题,是高考的“热点”之一。多年以来全国高考化学试卷年年涉及这种题型。这种题型考查的知识点多,灵活性、综合性较强,有较好的区分度,它能有效地测试出学生对强弱电解质、电离平衡、水的电离、pH、离子反应、盐类水解等基本概念的掌握及对这些知识的综合运用能力。
【正解】NH3・H2O是一元弱酸,属于弱电解质,在水溶液中少部分发生电离(NH3・H2O NH4++OH-),所以c(NH3・H2O)必大于c(NH4+)及c(OH-)。因为c(OH-)=c(NH4+)+C(H+),所以c(OH-)>c(NH4+)。综合起来,c(NH3・H2O)>c(OH-)>c(NH4+)c(H+),选择A选项。
NH4++OH-),所以c(NH3・H2O)必大于c(NH4+)及c(OH-)。因为c(OH-)=c(NH4+)+C(H+),所以c(OH-)>c(NH4+)。综合起来,c(NH3・H2O)>c(OH-)>c(NH4+)c(H+),选择A选项。
本题难度:一般
2、选择题 用水稀释0.1 mol・L-1的CH3COOH溶液,其中随水的量增加而增大的是
①c(H+) ②n(H+) ③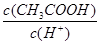 ④
④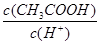 ⑤c(OH-) ⑥c(CH3COO-)
⑤c(OH-) ⑥c(CH3COO-)
A.①②③
B.②③⑤
C.④⑤
D.④⑤⑥
参考答案:B
本题解析:用水稀释0.1 mol・L-1的CH3COOH溶液,醋酸的电离平衡破坏,平衡正向移动,氢离子的物质的量增大,但是浓度减小,相应的氢氧根离子浓度增大,因此选B。
考点:考查弱电解质的电离。
本题难度:一般
3、填空题 A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中一种.常温下进行下列实验:
①将1LpH=3的A溶液分别与0.001mol?L-1xLB溶液、0.001mol?L-1yLD溶液充分反应后溶液呈中性,x、y大小关系为:y<x;
②浓度均为0.1mol?L-1A和E溶液,pH:A<E;
③浓度均为0.1mol?L-1C与D溶液等体积混合,溶液呈酸性.
回答下列问题:
(1)D是______溶液
(2)用水稀释0.1mol?L-1B时,溶液中随着水量的增加而减小的是______(填写序号)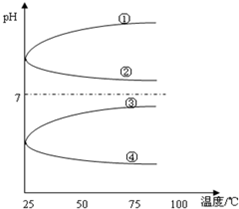
①
| c(B) c(OH-) |
| c(OH-) c(H+) |
参考答案:(1)中和酸性物质A只有NaOH、NH3?H2O,物质的量的A与等物质的量浓度B和D混合呈中性,D的用量少,说明D碱性比B的碱性强,所以D是NaOH,故答案为:NaOH;
(2)①、由NH3?H2O?OH-+NH4+可知,加水促进电离,则n(NH3?H2O)减少,n(OH-)增大,则C(NH3?H2O)C(OH-)=n(NH3?H2O)n(OH-)减小,故①错误;
②、由NH3?H2O?OH-+NH4+可知,加水促进电离,则n(NH3?H2O)减少,n(OH-)增大,c(NH3?H2O)、c(OH-)都减小,c(H+)减小,则c(OH-)c(H+)减小,故②正确;
③、因加水稀释时,温度不变,则c(H+)和c(OH-)的乘积不变,故③错误;
④、由NH3?H2O?OH-+NH4+可知,加水促进电离,OH-的物质的量增大,故④错误;
故答案为:①②;
(3)等体积、等物质的量浓度NH3?H2O和与NH4HSO4混合后溶液发生反应:NH3?H2O+NH4HSO4=(NH4)2SO4+H2O,NH4)2SO4要发生水NH4++H2O?NH3?H2O+H+,溶液呈酸性,加热水解平衡正向移动,c(H+)增大,pH减小,故答案为:④;
(4)①根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,产生的氢气一样多,反应所需要的时间HCl>CH3COOH,故①错误;
②根据酸能与锌反应得到氢气,开始溶液中c(H+)相等,反应时的速率HCl=CH3COOH,故②错误;
③根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故③正确;
④根据酸能与锌反应得到氢气,随着反应的进行,CH3COOH不断电离出H+,反应速率比盐酸中快,故④正确;
⑤根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑤正确;
⑥根据酸能与锌反应得到氢气,若最后仅有一份溶液中存在锌,放出氢气的质量相同,说明盐酸中锌剩余,CH3COOH中锌完全反应,参加反应的锌的物质的量相等,故⑥错误;
故答案为:③④⑤;
(5)NH4HSO4中滴入NaOH溶液,NaOH首先与NH4HSO4电离出的H+作用,因为H+结合OH-的能力比NH4+结合OH-的能量强(原因是产物H2O比NH3?H2O更难电离).当加入等摩尔的NaOH时,正好将H+中和,此时c(Na+)=c(SO42-),但此时溶液中还有NH4+,NH4+水解使溶液呈酸性,因此要使溶液呈中性,则还需继续滴入NaOH,当然到中性时c(OH-)=c(H+),c(Na+)>c(SO42- )>c(NH4+),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
本题解析:
本题难度:简单
4、选择题 关于溶液的酸性、酸性强弱的说法中,正确的是
A.只要溶液中有H+,溶液就显酸性
B.H+浓度大于OH-浓度,溶液一定显酸性
C.H+ 浓度增大,溶液的酸性一定增强
D.强酸溶液的酸性一定比弱酸溶液的酸性强
参考答案:B
本题解析:溶液的酸碱性主要由c(H+)和c(OH-)的相对大小决定,若c(H+)>c(OH-)溶液显酸性;若c(H+)<c(OH-)溶液显碱性;若c(H+)=c(OH-)溶液显中性。溶液的酸性只与溶液中c(H+)的相对大小有关,而与强酸及弱酸无关,因此答案是B。
本题难度:一般
5、选择题 在0.1mol・L-1CH3COOH溶液中存在如下电离平衡:CH3COOH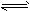 CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
[? ]
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1mol・L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
参考答案:B
本题解析:
本题难度:一般