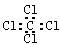时间:2017-09-25 16:22:56
1、填空题 按要求书写电子式。
a.原子电子式的书写:H____;Mg____;Al______; C______;N____;O____; F____;Ne_____;
b.简单阳离子电子式的书写:钠离子______;镁离子______;铝离子______;氢离子______;
c.简单阴离子电子式的书写:硫离子______;氯离子______;氧离子______; 氢负离子______;
d.离子化合物的电子式书写:MgO_______,Na2S_______ K2S:_______;CaF2_______;
e.用电子式表示离子键的形成过程:KBr_______;MgCl2_______;K2O_______
2、选择题 最近日本科学家确认世界上还存在的另一种“分子足球”N60,它与C60的结构相似。下列说法正确的是(?)
A.N60是一种新型化合物
B.N60和14N都是氮的同位素
C.N60和N2是同素异形体
D.N60和N2是同分异构体
3、选择题 下列说法中错误的是?(?)
A.键长越短,键能越大,分子越稳定
B.分子的性质与键角无关
C.分子具有一定的键角,表明共价键具有方向性,由键角可知分子的形状
D.π键的电子云形状的特征为镜象对称,σ键的电子云形状的特征为轴对称
4、简答题 有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻
的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在右表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
(1)A、B、D、E四种元素分别与M元素形成的简单化合物中,沸点最高的是______(填化学式).
(2)M、D、E、N形成的简单离子的半径由大到小的关系是(写离子符号)______.
(3)A、B、D、M可组成多种18电子分子,请写出1种具有18电子的有机物的分子式______.
(4)由A、D、N三种元素组成的无机物,其水溶液呈碱性,用离子方程式表示其原因______.
(5)元素B的氢化物与元素D单质在一定条件下发生置换反应,在该反应中氧化剂与还原剂的物质的量之比为______.
(6)在由M、D、N、E四种元素构成的化合物的水溶液中滴入少量的Ba(OH)2溶液,写出可能发生的所有反应的离子方程式______.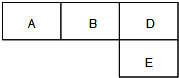
5、选择题 下列化学用语表达正确的是
[? ]
A.乙酸的分子式:CH3-COOH
B.丙烷分子的球棍模型: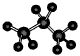
C.Ar原子的结构示意图: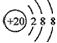
D.四氯化碳的电子式: