时间:2017-09-24 00:34:30
1、选择题 常温下pH=3的二元弱酸H2R溶液与a L pH=11的NaOH溶液混合后,混合液的pH刚好等于7(假设反应前后体积不变),则对反应后混合液的叙述正确的是
A.c(R2-)+ c(OH-)=c(Na+)+c(H+)
B.c(R2-)>c(Na+)>c(H+)=c(OH-)
C.混合后溶液的体积为2aL
D.2c(R2-)+ c(HR-)=c(Na+)
参考答案:D
本题解析:电荷守恒的关系式为2c(R2-)+c(HR-)+ c(OH-)=c(Na+)+c(H+),A错误。
混合液的pH刚好等于7,溶液为中性,c(H+)=c(OH-),再根据电荷守恒可知2c(R2-)+ c(HR-)=c(Na+),可推出:c(R2-)<c(Na+),故B错误,D正确。二元弱酸H2R溶液的体积不等于a L,若等于a L,则反应后的溶液应显酸性,故二元弱酸H2R溶液的体积应小于a L,混合后溶液的体积小于2aL,C错误。
故选D
本题难度:一般
2、选择题 下列式子中,属于水解反应的是( )
A.H2O+H2O?H3O++OH-
B.CO32-+H2O?HCO3-+OH-
C.NH3+H2O?NH3?H2O
D.HCO3-+OH-?H2O+CO32-
参考答案:B
本题解析:
本题难度:简单
3、选择题 常温下0.1mol/L碳酸溶液中,下列离子关系式正确的是
A.c(H+)=2 c(CO32-)+c(OH-)
B.0.1= c(HCO3-)+2c(CO32-)
C.c(OH-)= c(H+) - c(HCO3-)-2 c(CO32-)
D.c(H+)>c(CO32-) > c(HCO3-)
参考答案:C
本题解析:选项A不正确,不符合电荷守恒定律,应该是c(H+)=2 c(CO32-)+c(OH-)+c(HCO3-),因此选项C正确;选项B不正确,不符合物料失衡,应该是0.1= c(HCO3-)+c(CO32-)+c(H2CO3);碳酸的第二步电离程度很小,选项D不正确,应该是c(H+) > c(HCO3-)>c(CO32-),答案选C。
本题难度:一般
4、选择题 常温下,用0.1000 mol/L HCl溶液滴定20.00 mL 0.1000 mol/L NH3?H2O溶液,滴定曲线如下图。下列说法正确的是
A.①溶液:c(C1―)>c(NH4+)>c(OH―)>c(H+)
B.②溶液:c(NH4+)=c(C1―)>c(OH―)=c(H+)
C.③溶液:c(H+)>c(NH3・H2O) + c(OH―)
D.滴定过程中可能出现:c(NH3?H2O)>c(NH4+)>c(OH―)>c(Cl―)>c(H+)
参考答案:BD
本题解析:根据电荷守恒c(C1―)+c(OH―)=c(NH4+)+c(H+)可知,A不正确。②表示溶液显中性,根据电荷守恒可判断,B正确。③表示盐酸和氨水恰好反应,溶液中只有氯化铵,水解显酸性。根据质子守恒可知,c(H+)=c(NH3・H2O) + c(OH―),C不正确。当加入的盐酸很少时,可能出现选项D中的关系,所以答案选BD。
本题难度:困难
5、填空题 (共14分)甲醇是重要的化学工业基础原料和液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
| 化学反应 | 平衡常数 | 温度(℃) | |
| 500 | 800 | ||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
③3H2(g)+ CO2(g) CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |
参考答案:(共14分)
(1)吸热(1分)
(2)=(1分)
(3)< 、<(各2分);>(2分)
(4)加入催化剂(2分);
将容器的体积快速压缩至2L(2分,只写出加压或缩小容器体积得1分)
(5) c(CH3COO-)>c(Ba2+)>c(OH-)>c(H+)(2分)
本题解析:(1)对于反应②,温度升高,平衡常数增大,说明升高温度对正反应有利,所以该反应是吸热反应;
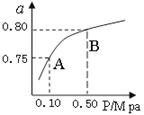
(2)平衡常数是温度常数,只随温度变化,所以A、B点的温度相同,平衡常数也相同,K(A)=K(B)
(3)反应③=反应①+反应②,所以K3=K1・K2,500℃K3=2.5,800℃ K3=0.375,温度升高,平衡常数减小,说明温度升高对逆反应有利,正向是放热反应,所以△H<0,由化学方程式的系数可知,反应物中气体的总系数是4,生成物的总系数是2,所以△S<0;
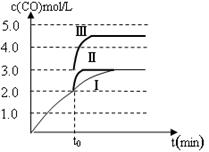
(4)t0时刻曲线Ⅰ变为曲线Ⅱ时,CO的浓度未变,到达平衡的时间缩短,说明反应速率加快,平衡不移动,所以改变的条件是加入催化剂;曲线Ⅰ变为曲线Ⅲ时,CO的浓度由2.0mol/L增大到3.0mol/L,浓度增大1.5倍,说明容器的体积由原来的3L迅速缩小1.5倍,变为2L,达平衡时CO的浓度是4.5mol/L,所以改变的条件只能是将容器的体积快速压缩至2L;
(5)0.2 mol/L的乙酸与0.1 mol/LBa(OH)2溶液等体积混合,醋酸与氢氧化钡恰好完全反应,生成醋酸钡溶液,尽管醋酸根离子水解,但醋酸根离子浓度仍大于钡离子浓度,水解使溶液显碱性,所以离子浓度的大小关系是c(CH3COO-)>c(Ba2+)>c(OH-)>c(H+)。
考点:考查化学热效应的判断,化学平衡常数的应用,图像的分析,溶液的离子浓度的比较
本题难度:困难