时间:2017-09-24 00:07:22
1、填空题 根据下图推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为________;每个Cs+周围距离相等且次近的Cs+数目为________,距离为________;每个Cs+周围距离相等且第三近的Cs+数目为________,距离为________;每个Cs+周围紧邻且等距的Cl-数目为________。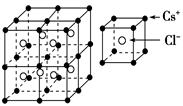
参考答案:6? 12 ?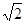 a? 8 ?
a? 8 ?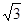 a? 8
a? 8
本题解析:根据氯化铯的晶胞可知,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为6个(即上下、左右和前后各1个);每个Cs+周围距离相等且次近的Cs+位于面心处,数目为(3×8)÷2=12个,距离为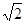 a;每个Cs+周围距离相等且第三近的Cs+位于体心处,数目为8个,距离为
a;每个Cs+周围距离相等且第三近的Cs+位于体心处,数目为8个,距离为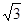 a;由于定点被8个相邻的正方体共用,所以每个Cs+周围紧邻且等距的Cl-数目为8个。
a;由于定点被8个相邻的正方体共用,所以每个Cs+周围紧邻且等距的Cl-数目为8个。
点评:该题是知道你的的试题,试题贴近高考,基础性强,侧重对学生能力的培养旨在培养学生分析、归纳和总结问题的能力,有利于调动学生的学习兴趣,激发学生的学习积极性,提高学生的应试能力。
本题难度:一般
2、填空题 人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”.试回答下列问题:? 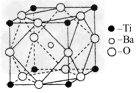
(1)Ti元素在元素周期表中的位置是第________周期第________族;其基态原子的价电子排布为________.
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定.
①偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如图所示,它的化学式是________.
②已知Ti3+可形成配位数为6的配合物.现有含钛的两种颜色的晶体,一种为紫色,另一种为绿色,但相关实验证明,两种晶体的组成皆为TiCl3・6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液与AgNO3溶液反应得到的沉淀质量的2/3. 则绿色晶体配合物的化学式为____________________,绿色晶体中含有的化学键类型是________.
参考答案:(1)四;ⅣB;3d24s2
(2)①BaTiO3;②[TiCl(H2O)5]Cl2・H2O;共价键、配位键、离子键
本题解析:
本题难度:一般
3、选择题 下列说法不正确的是?
A.氯化钠晶体中,每个Cl-周围最近且距离相等的Cl-共有12个
B.分子晶体中有范德华力,也有共价键
C.干冰晶体中,每个CO2分子周围最近且距离相等的CO2分子共有12个
D.晶体熔点:晶体硅<SiC
参考答案:B
本题解析:A.氯化钠晶体中,每个Cl-周围最近且距离相等的Cl-的个数是:(3×8)÷2=12个。正确。B.在分子晶体中有范德华力,若分子为单原子分子,则分子内无共价键,若为双原子分子或多原子分子,则也有共价键。错误。C.干冰晶体中,每个CO2分子周围最近且距离相等的CO2分子个数为:(3×8)÷2=12个。正确。D.晶体Si、SiC但是原子晶体。对于原子晶体来说,共价键的键长越短,则共价键结合的就越牢固,断裂消耗的能量就越高,熔沸点就越高。而键长取决于形成共价键的原子半径,由于原子半径Si>C,晶体熔点:晶体硅<SiC。正确。
本题难度:一般
4、填空题 (8分)(1)某晶体的晶胞如图所示,X位于体心,Y位于6面心,Z位于顶点,该晶体中 X、Y、Z的粒子个数比为____? _? __;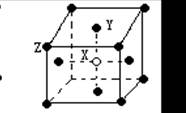
(2)Co(NH3)5BrSO4可形成两种钴的配合物,已知两种配合物的分子式分别为[Co(NH3)5Br] SO4和[Co (SO4) (NH3)5] Br,在第一种配合物的溶液中加BaCl2溶液时,现象是?;如果在第二种配合物的溶液中加入BaCl2溶液时,现象是?,若在第二种配合物的溶液加入 AgNO3溶液时,现象是?。
参考答案:(1)1:3:1(2)白色沉淀无明显现象淡黄色沉淀
本题解析:处于顶点的粒子:同时为8个晶胞共用,每个粒子有1/8属于该晶胞;处于棱上的粒子:同时为4个晶胞共用,每个粒子有1/4属于该晶胞;处于面上的粒子:同时为2个晶胞共用,每个粒子有1/2属于该晶胞;处于晶胞内部的粒子:完全属于该晶胞。
(1)X=1;Y=6×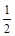 =3;Z=8×
=3;Z=8×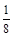 ;
;
(2)由[Co(NH3)5Br]SO4可知,硫酸根离子为配合物的外界,在水溶液中以离子形式存在,所以会与钡离子结合成白色沉淀.加入BaCl2溶液时,无明显现象,说明硫酸根离子在内界,若加入AgNO3溶液时,产生淡黄色沉淀,说明溴离子在外界.
本题难度:一般
5、选择题 下列变化过程中,克服的是分子间作用力的是(?)
A?烧碱溶于水? B?氯化氢气体溶于水
C?二氧化碳变成干冰? D?加热碘化氢使其分解
参考答案:C
本题解析:烧碱溶于水克服离子键;氯化氢气体溶于水,克服共价键;二氧化碳变成干冰发生物理变化克服分子间作用力;碘化氢分解发生化学变化,克服共价键。选C。
本题难度:一般