时间:2017-09-24 00:04:20
1、选择题 为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1克样品加热,其质量变为w2g,则该样品的纯度(质量分数)是
[? ]
A.
B.
C.
D.
参考答案:A
本题解析:
本题难度:一般
2、计算题 有一定质量的Zn与100 mL 18.5 mol·L-1的浓硫酸充分反应,Zn完全溶解,同时生成标准状况下的气体A
33.6 L,将反应后的溶液稀释到1 L,测得溶液中H+的浓度 为0.1 mol·L-1。求气体A中各组分的体积比。
参考答案:反应后溶液为1L,H+的浓度为0.1 mol·L-1,则 n(H+) =0.1 mol·L-1×1 L =0.1 mol,
故反应后溶液中剩余硫酸0.05 mol。由于浓硫酸与Zn反应过程中有水生成,溶液变稀,故有H2、SO2两种气体产生。
设SO2 .H2的物质的量分别为 x、y,则:
Zn+H2SO4=ZnSO4+ H2↑
? y?y
Zn+2H2SO4 (浓) ZnSO4 +SO2↑+2H2O
ZnSO4 +SO2↑+2H2O
2x? x 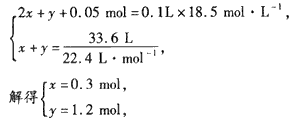
所以A气体中V(SO2):V(H2)=0.3 mol: 1.2 mol=1:4。
本题解析:
本题难度:一般
3、选择题 等体积.等物质的量浓度的硫酸.氢氧化钠溶液分别放在甲.乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲.乙两烧杯中的反应情况可能分别是
[? ]
A.甲.乙中都是铝过量
B.甲中铝过量.乙中碱过量
C.甲中酸过量.乙中铝过量
D.甲中酸过量.乙中碱过量
参考答案:B
本题解析:
本题难度:一般
4、选择题 甲,乙两只烧杯中各盛有100 ml 3 mol/L的盐酸和氢氧化钠溶液,向两只烧杯中分别加入等质量的铝粉,反应结束后测得生成气体的体积比V(甲):V(乙)=1:2,则加入铝粉的质量为
A5.4 g
B 3.6 g
C 2.7 g
D 1.8 g
参考答案:A
本题解析:
本题难度:一般
5、选择题 足量铜与一定量的浓硝酸反应后得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2 (标准状况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
[? ]
A.60 mL
B.45 mL
C.30 mL
D.15 mL
参考答案:A
本题解析:
本题难度:一般