时间:2017-09-23 23:45:53
1、实验题 (14分)(Ⅰ)FeCl3的水溶液呈________(填“酸性”、“碱性”或“中性”),原因是__________________________________(用离子方程式表示);实验室配制FeCl3的水溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以___________(填“促进”、“抑制”)其水解;如果把FeCl3溶液蒸干,灼烧,最后得到的主要固体产物是____________________。
(Ⅱ)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①用0.10mol/L的标准盐酸润洗酸式滴定管2~3次
②取标准盐酸注入酸式滴定管至“0”刻度以上2~3mL处
③把盛有标准盐酸的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液
④调节液面至“0”或“0”刻度以下,记下读数
⑤取20.00mL待测NaOH溶液注入洁净的锥形瓶中,并加入2~3滴甲基橙试液
⑥把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点,记录滴定管读数
请回答下列问题:
(1)某次滴定时的滴定管中的液面如右图所示,其读数为 ?mL。
(2)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |
2、选择题 下列溶液一定呈酸性的是
A:KW=10-13的溶液? B:含少量OH-的溶液
C:含少量H+的溶液? D:C(H+) >C(OH-)的溶液
3、选择题 在Na2SO4、NaCl、NaOH的混合溶液中,Na+、SO42-、OH-的个数比是8:1:2,则溶液中Na2SO4、NaCl、NaOH的物质的量之比是?
A.1:1:1
B.1:4:2
C.1:2:4
D.1:3:2
4、选择题 下列说法不正确的是?(?)
①用润湿的pH试纸测定溶液的pH时,一定会产生误差
②明矾、胆矾、冰醋酸、硫酸钡、硫酸钠均为电解质
③某温度下测得纯水的c(H+)=2×10-7mol/L,则其中的c(OH-)=5×10-5mol/L
④所有的燃烧反应都为放热反应
A.仅有①④
B.仅有②③
C.仅有①③
D.全不正确
5、判断题 氢气是未来的最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O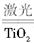 2H2↑+O2↑。制得的氢气可用于燃料电池。试完成下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试完成下列问题:
(1)分解海水时,实现了从_________________能转变为_________________能,二氧化钛作______________。生成的氢气,用于燃料电池时,实现______________能转变为_____________能。水分解时,断裂的化学键有______________,分解海水的反应属于______________反应(填“放热”或“吸热”)。
(2)某种氢燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:H2+O2-====H2O+2e-;B极:O2+4e-====2O2-
则A极是电池的______________极;电子从该______________极(填“流入”或“流出”)。