时间:2017-09-23 23:37:58
1、简答题 A、B、C、D四种元素,A元素所处的周期数,主族序数,原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称______,B在周期表中的位置______,
(2)A、B形成的化合物的电子式______;
(3)C的元素符号______,C的最高价氧化物的化学式______;
(4)D的最高价氧化物的水化物中含有______键.
(5)用电子式表示D2C的形成过程:______.
2、填空题 周期表中前四周期中的六种元素A、B、C、D、E、F原子序数依次增大,已知A原子2p轨道有3个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体熔点在同周期形成的单质中是最高的;F2+核外各电子层电子均已充满。
根据以上信息回答下列问题:
(1)写出D原子核外电子排布式:____________________________________________。
(2)A、B、C、D的第一电离能由小到大的顺序为________________________________(用元素符号表示)。
(3)B的氯化物的熔点比D的氯化物的熔点________(填“高”或“低”);理由是_______________________________________________________。
(4)E的最高价氧化物分子的空间构型是________,是________(填“极性”或“非极性”)分子。
(5)E、F形成的某种化合物有如图所示的晶体结构:该化合物化学式为________;E原子配位数为________________________________________________。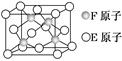
3、选择题 下列说法不正确的是
[? ]
A.共价化合物和离子化合物中,一定都含有非金属元素
B.一个化学反应的过程,本质上就是旧化学键断裂和新化学键形成的过程
C.全部由非金属构成的化合物一定不存在离子键
D.共价化合物都是由分子构成的,而离子化合物中一般不存在单个分子
4、选择题 下列表达方式错误的是( )
A.CO2的分子模型示意图:
B.HClO的路易斯结构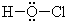
C.sp3杂化道图: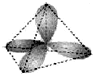
D.π电子云图:
5、选择题 关于下列说法正确的是(? )
A.加热氯化铵与固化碘过程中发生的都是升华
B.氢键的存在主要影响物质的物理性质,如熔沸点和在水中的溶解度
C.水分子相当稳定是因为水分子间存在很强的分子间作用力
D.直接由原子构成的晶体必然是原子晶体