时间:2017-08-26 02:55:59
1、选择题 用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是
[? ]
A.上下移动①中铜丝可控制SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向①中加水,观察颜色
参考答案:D
本题解析:
本题难度:一般
2、实验题 (8分)欲配制100mL 0.2mol/L的NaOH溶液,回答下列问题:
(1) (2分)根据计算,所需的NaOH的质量为?,NaOH固体应放在?中称量。(2) (3分)以下是实验操作步 骤,请排出正确的操作顺序:
骤,请排出正确的操作顺序:
①称取所需质量的NaOH
②将溶液转移到容量瓶内
③用蒸馏水洗涤烧杯2~3次,将洗涤液全部移入容量瓶中,摇匀
④改用胶头滴管,小心滴入蒸馏水至刻度
⑤仔细地把蒸馏水注入容量瓶中,直到液面接近刻度线1cm~2cm处
⑥塞上瓶塞。反复摇匀
⑦将称取的NaOH置于烧杯内,加适量蒸馏水,搅拌溶解后冷却
正确的操作顺序是:??
(3) (3分)下列操作会使所配溶液浓度偏低的是?(填选项代号)
A.NaOH放在纸上称量,且出现潮解现象
B.配制前容量瓶内已有少量蒸馏水
C.定容时仰视
D.NaOH溶液未经冷却就转移到容量瓶中去
E.转移溶液时部分溶液溅出容量瓶外
参考答案:(1)(2分)0.8g?,小烧杯。(2)(3分)①⑦②③⑤④⑥(3) (3分) ACE
本题解析:略
本题难度:一般
3、实验题 (18分)
硫酸铜是一种应用极其广泛的化工原料.某课外兴趣小组将适量浓硝酸分多次加到铜粉与稀?硫酸的混合物中,加热使之反应完全(装置如题29图I、图Ⅱ所示),通过蒸发、结晶得到硫酸铜晶体,并同时测定硫酸铜晶体中结晶水的含量.
(1)怎样检查图I装置的气密性?。
(2)图I中分液漏斗内装的液体是?。
(3)图Ⅱ是图Ⅰ的改进装置,与图I相比,图Ⅱ装置的明显优点是?,
?,?,(可不答满).
(4)课外兴趣小组同学在测定胆矾 晶体中结晶水的含量时.测得有关数据如下表:
晶体中结晶水的含量时.测得有关数据如下表:
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水CuSO4) |
| 5.4g | 7.9g | 6.8g |

 中结晶水含量的实验中,称量操作至少进行?次。
中结晶水含量的实验中,称量操作至少进行?次。 相比
相比 )?(填“偏高”、“偏低”、“不变”),可能的原因是?。(填字母序号)
)?(填“偏高”、“偏低”、“不变”),可能的原因是?。(填字母序号)参考答案:
(1)连接好装置,关闭分液漏斗活塞,将导气管插入盛水的烧杯中,用酒精灯微热烧瓶,导气管中有气泡产生,停止微热后导管中形成一段水柱,则气密性好.?(3分)
(2)浓硝酸?(2分)
(3)防止倒吸,(1分)有害气体能被完全吸收(1分)
(4)①坩埚钳、干燥器、玻璃棒(写出药匙、研钵不算错)?(3分)
②再次加热冷却称量,直到连续两次称量的质量差不超过0.lg?(2分)
③4?(2分)
④偏高,(2分)? a?(2分)
本题解析:略
本题难度:一般
4、实验题 某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。其实验流程图如下: 
(1)测定硝酸的物质的量?
反应结束后,从下图B装置中所得100mL溶液中取出25?.00mL溶液,用0.1mol?L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如右上图所示。在B容器中生成硝酸的物质的量为_____________?mol。?
(2)测定NO的体积?
①从上图所示的装置中,你认为应选用___________装置进行Cu与浓硝酸反应实验,选用的理由是____________?。 ?
②选用上图所示仪器组合一套可用来完成实验并测定生成NO体积的装置,其合理的连接顺序是(填各导管口编号)_______________。 ?
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置?________________(“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。?
(3)气体成分分析:若实验测得NO的体积为112.0mL(已折算到标?准状况),则Cu与浓硝酸反应的过程中____________(填“有”或“没有”)NO产生,作此判断的依据是___________。?
(4)实验前,用托盘天平称取的铜片至少应为____________g。
参考答案:(1)0.008?
(2)A ;因为A装置可以通N2 装装置中的空气排尽,防止反应生成的NO被装置内空气中O2?
装装置中的空气排尽,防止反应生成的NO被装置内空气中O2?
②123547?
③升高
(3)有 ;因为NO2与水反应生成的NO 的体积小于收集到的NO 的体积(89.6mL<112.0mL )
(4)0.5
本题解析:
本题难度:困难
5、实验题 某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下: 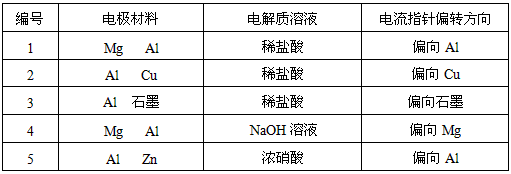
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极是否相同?____________。
(2)写出实验3中的电极反应式。
铝为( )_____________________________________;
石墨为( )___________________________________;
(3)实验4中的铝作正极还是负极?写出电池总反应方程式。
________________________________________
(4)解释实验5中电流指针偏向铝的原因。
________________________________________
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受哪些因素的影响?
________________________________________
参考答案:
(1)不同
(2)负极;2Al-6e-==2Al3+;正极;6H++6e-==3H2↑
(3)负极;电池总反应式:2Al+2NaOH+6H2O==2Na[Al(OH)4]+3H2↑
(4)由于铝在浓硝酸中发生钝化,反以锌为负极
(5)与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关
本题解析:
本题难度:困难