时间:2017-08-26 00:56:19
1、选择题 配制一定物质的量浓度溶液时,能使所配溶液的浓度偏高的原因是( )
A.没有用水冲洗烧杯2-3次
B.溶液配好摇匀后,发现液面低于刻度线,又加水至液面与刻度线相切
C.定容时俯视液面使与刻度线相切
D.定容时仰视液面使与刻度线相切
参考答案:C
本题解析:
本题难度:一般
2、实验题 超细氧化铝是一种重要的功能陶瓷原料。
(1)实验室常以NH4Al(SO4)2和NH4HCO3为原料,在一定条件下先反应生成沉淀NH4AlO(OH)HCO3,该沉淀高温分解即得超Al2O3,NH4AlO(OH)HCO3热分解的化学反应方程式_______________________。
(2)NH4Al(SO4)2・12H2O的相对分子质量为453。欲配制100mlPH为2浓度约为0.1mol-1的NH4Al(SO4)2溶液,配制过程为
①用托盘天平称量NH4Al(SO4)2・12H2O固体__________g。
②将上述固体置于烧杯中______________________________。
(3)在0.1mol・L-1 NH4Al(SO4)2溶液中,铝各形态的浓度(以Al3+计)的对数(lgc)随溶液pH变化的关系
见下图 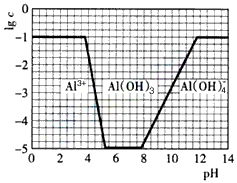
①用NaOH溶液调节(2)中溶液pH至7,该过程中发生反应的离子方程式有_______________________
②请在答题卡的框图中,画出0.01mol・L-1NH4Al(SO4)2溶液中铝各形态的浓度的对数lgc随溶液pH变化的关系图,并进行必要的标注。
参考答案:(1)2NH4AlO(OH)HCO3 2NH3↑+Al2O3+3H2O↑+2CO2↑
2NH3↑+Al2O3+3H2O↑+2CO2↑
(2)4.5g;边加蒸馏水溶解边用玻璃棒搅拌,待完全溶解后,用玻璃棒移液至100mL的容量瓶中,用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转移到容量瓶中,加蒸馏水至刻度线2~3cm处应改用胶头滴管,上下振荡,静置,将配置好的溶液装入试剂瓶中,并贴上标签。
(3)“略”
本题解析:
本题难度:一般
3、填空题 用18mol?L-1浓硫酸配制100mL2.8mol?L-1稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸③稀释④转移⑤洗涤 ⑥定容⑦摇匀
完成下列问题:
(1)所需浓硫酸的体积是______(小数点后保留一位数字).
(2)该实验用到的仪器除量筒、烧杯外还需的定量仪器有______,该仪器上需标有以下五项中的______(用序号填写)
①温度②浓度③容量④压强⑤刻度线
(3)第⑤步实验的目的是______.
(4)下列情况对所配制的稀硫酸浓度有何影响?(用“偏高”“偏低”“无影响”填写)?
①用量筒量取浓硫酸时俯视刻度______.
②容量瓶用蒸馏水洗涤后未干燥______.
③浓硫酸稀释后未冷却即转移、定容______.
参考答案:配制100ml 2.8mol/L 稀硫酸,需要18mol/L 浓硫酸的体积为:2.8mol/L×0.1L18mol/L≈0.0156mL=15.6mL,
故答案为:15.6mL;
(2)配制100ml 2.8mol/L 稀硫酸,配制的步骤为:计算、稀释、冷却、转移、洗涤、定容、摇匀等,使用的玻璃仪器有:玻璃仪器除烧杯、玻璃棒、量筒,还需100mL容量瓶,量瓶上标有刻度线、温度和容量;
故答案为:100mL容量瓶;①③⑤;
(3)溶解过程中,烧杯玻璃棒都有沾的溶质,洗涤保证溶质全部转移到容量瓶;
故答案为:把溶质全部转移至容量瓶;
(4)①量取浓硫酸时,若俯视液面,浓硫酸的体积偏少,溶质的物质的量偏小,所配溶液浓度偏低;
②最后需要加水和定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
③浓硫酸溶于水会放出大量的热量,若未冷却直接转移定容,由于热胀冷缩导致所配溶液体积偏小,故浓度偏高,
故答案为:偏低;无影响;偏高.
本题解析:
本题难度:一般
4、实验题 用质量分数为36.5%的浓盐酸(密度为1.16g/cm3)配制成1mol/L的稀盐酸。现实验室仅需要这种盐酸220mL。试回答下列问题:
(1)配制稀盐酸时,应选用的容量瓶规格是________(填序号)。 ?
A.25mL?B.50mL?C.100mL?D.250mL
(2)经计算需要______mL浓盐酸,在量取时宜选用下列量筒中的_______(填序号)。?
A.5mL?B.10mL?C.25mL?D.50mL
(3)在量取浓盐酸后,进行了下列操作: ?
①等稀释的盐酸其温度与室温一致后,沿玻璃棒注入容量瓶中。 ?
②往容量瓶中小心加蒸馏水至液面接近环形标线2~3?cm处,改用胶头滴管加蒸馏水,使溶液的凹面底部与瓶颈的环形标线相切。 ?
③在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。 ?
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)____________。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是_________(填“偏高”、“偏低”、“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是_________(填“偏高”、“偏低”、“无影响”)。
参考答案:(1)D
(2)21.6;C
(3)③①④②
(4)偏低;偏低
本题解析:
本题难度:一般
5、选择题 将V?L(标准状况)氯化氢气体溶于0.2L水中,所得盐酸溶液的密度是a?g/cm3,则所得盐酸溶液的物质的量浓度(mol/L)为
A.
B.
C.
D.
参考答案:B
本题解析:分析:根据n=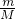 计算氯化氢气体的物质的量,再根据m=nM计算氯化氢气体的质量,溶液质量=气体质量+水的质量,利用V=
计算氯化氢气体的物质的量,再根据m=nM计算氯化氢气体的质量,溶液质量=气体质量+水的质量,利用V=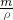 来计算溶液的体积,根据c=
来计算溶液的体积,根据c=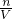 计算该气体的物质的量浓度.
计算该气体的物质的量浓度.
解答:标准状况下,将VL氯化氢的物质的量为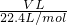 =
=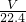 mol,
mol,
所以氯化氢气体的质量为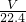 mol×36.5g/mol=
mol×36.5g/mol=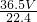 g,
g,
所以溶液的质量为200ml×1g/ml+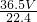 g=(200+
g=(200+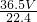 )g,
)g,
所以溶液的体积为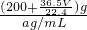 =
=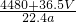 mL,
mL,
所以物质的量浓度为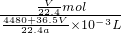 =
=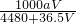 mol/L.
mol/L.
故选B.
点评:本题考查物质的量浓度的计算,难度不大,根据物质的量浓度的定义式计算,要根据溶液m=ρV正确判断溶液的体积,注意不能把溶剂的体积当做溶液的体积.
本题难度:简单