时间:2017-08-26 00:33:28
1、选择题 下列说法中,正确的是
A.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止
B.Ksp越小,难溶电解质在水中的溶解能力一定越弱
C.Ksp的大小与离子浓度无关,只与难溶电解质的性质和温度有关
D.相同温度下, AgCl在水中的溶解能力与在NaCl溶液中的相同
参考答案:C
本题解析:
正确答案:C
A.不正确,难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解仍在进行,只是沉淀速率等于溶解速率;
B.不正确,当物质的组成相似时,Ksp越小,难溶电解质在水中的溶解能力一定越弱;
C.正确;
D.不正确,相同温度下, AgCl在水中的溶解能力比在NaCl溶液中大,NaCl溶液中Cl―浓度大,抑制AgCl溶解。
本题难度:简单
2、选择题 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。
已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-)。下列说法正确的是
A.该温度下,Ksp (BaSO4 )=1.0×10-24
B.a点的Ksp (BaSO4 )小于b点的Ksp (BaSO4 )
C.d点表示的是该温度下BaSO4的不饱和溶液
D.加入BaCl2可以使溶液由 c点变到a点
参考答案:D
本题解析:A、硫酸钡电离产生硫酸根离子和钡离子,a点时p(Ba2+)=-lgc(Ba2+)=4,则c(Ba2+)=10-4mol/L,p(SO42-)=-lgc(SO42-)=6,则c(SO42-)=10-6mol/L,所以该温度下,Ksp (BaSO4 )= c(Ba2+) c(SO42-)=1.0×10-10,错误;B、温度相同,硫酸钡的溶度积相同,错误;C、因为p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-)是减函数,数值越小,则对应的两种浓度越大,所以d点时c(Ba2+) c(SO42-)>1.0×10-10,则溶液为过饱和溶液,错误;D、c点时加入氯化钡溶液,则溶液中的钡离子浓度增大,p(Ba2+)减小,则溶解平衡逆向移动,硫酸根离子浓度减小,p(SO42-)增大,可由c点变到a点,正确,答案选D。
考点:考查对沉淀溶解平衡图像的分析判断
本题难度:一般
3、填空题 (8分)氢氧化铜悬浊液中存在如下平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),常温下其Ksp=c(Cu2+)· c2(OH-)=2×10-20mol2·L-2。
Cu2+(aq)+2OH-(aq),常温下其Ksp=c(Cu2+)· c2(OH-)=2×10-20mol2·L-2。
(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH使之大于 。
(2)要使0.2mol/L硫酸铜溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为 。
参考答案:(1)5?(2)6
本题解析:考查溶度积常数和pH的有关计算。
(1)根据氢氧化铜的溶度积常数表达式可知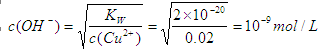 ,所以氢离子浓度为10-5mol/L,因此pH等于5。
,所以氢离子浓度为10-5mol/L,因此pH等于5。
(2)Cu2+浓度降至原来的千分之一后,铜离子的浓度变为2×10-4mol/L,所以根据氢氧化铜的溶
度积常数表达式可知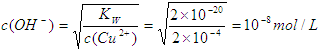
所以氢离子浓度为10-6mol/L,因此pH等于6。
本题难度:简单
4、填空题 (13分)Ⅰ、短周期元素X、Y、Z在元素周期表中的相对位置如下图所示。
| | | | X |
| Y | | | Z |
 H2(g) + CO2(g)的平衡常数随温度的变化如下表:
H2(g) + CO2(g)的平衡常数随温度的变化如下表:| 温度/℃ | 400 | 500 |
| 平衡常数 | 9.94 | 9 |
 Ni(CO)4(g),ΔH<0。
Ni(CO)4(g),ΔH<0。参考答案:
I、(1)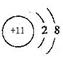 ;
;
(2)CH4
(3)SiO2+2OH-=SiO32-+H2O
(4)SiO2+C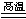 Si+CO↑
Si+CO↑
(5)KA+CO2+H2O=HA+KHCO3
II、(6)放热
(7)K=c(H2)c(CO2)/c(CO)c(H2O)
(8)40%;1
(9)C
本题解析:I、25℃,0.1 mol·L-1M溶液(M为Y的最高价氧化物的水化物)的pH为13,说明M是强碱,根据X、Y、Z在元素周期表中的位置判断Y是Na元素,对应的最高价氧化物的水化物是氢氧化钠,为强碱;则X是C元素,Z是Si元素。
(1)Na的离子结构示意图为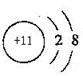 ;
;
(2)C的非金属性大于Si,所以C的气态氢化物CH4的稳定性较强;
(3)因为氢氧化钠与玻璃塞中的二氧化硅反应生成粘性较大的硅酸钠,所以不能用带磨口玻璃塞的试剂瓶盛装氢氧化钠溶液,离子方程式是SiO2+2OH-=SiO32-+H2O;
(4)工业上用单质碳还原二氧化硅制取Si单质,化学方程式是SiO2+C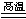 Si+CO↑;
Si+CO↑;
(5)根据所给酸的电离常数可知,酸性H2CO3>HA>HCO3-,所以二氧化碳与KA溶液反应只能生成碳酸氢钾和HA,则化学方程式是KA+CO2+H2O=HA+KHCO3。
II、(6)温度升高,平衡常数减小,说明升高温度,平衡逆向移动,则该反应是放热反应;
(7)根据平衡常数的定义,该反应的平衡常数K=c(H2)c(CO2)/c(CO)c(H2O);
(8)830K时,若起始时:C(CO)=2mol/L,C(H2O)=3mol/L,平衡时CO的转化率为60%,则平衡时c(H2)=c(CO2)=2mol/L×60%=1.2mol/L,消耗水蒸气的浓度也是1.2mol/L,则水蒸气的转化率为1.2mol/L/3mol/L×100%=40%;平衡时水蒸气的浓度是3mol/L-1.2mol/L=1.8mol/L,CO的浓度是2mol/L-1.2mol/L=0.8mol/L,代入K=c(H2)c(CO2)/c(CO)c(H2O),则该温度下的平衡常数是1.22/(0.8×1.8)=1;
(9)A、Ni为固体,增加Ni的量,平衡不移动,CO的转化率不变,错误;B、缩小容器容积,压强增大,平衡右移,但ΔH不变,错误;C、反应达到平衡后,充入CO,相当于增大压强,平衡正向移动,则再次达到平衡时,CO的体积分数减小,正确;D、因为该反应有固体参加,气体的总质量分数变化,达到平衡时气体的质量不再变化,则气体的密度不变,所以当容器中混合气体密度不变时,可说明反应已达化学平衡状态,而4v正[Ni(CO)4]= v正(CO)表示正反应速率,不符合正逆反应速率相等的特征,不能判断平衡的到达,错误,答案选C。
考点:考查元素推断,化学用语的书写,化学平衡的移动机平衡常数的应用
本题难度:困难
5、选择题 向5 mL NaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系为(? )
A.AgCl=AgI=Ag2S
B.AgCl<AgI<Ag2S
C.AgCl>AgI>Ag2S
D.AgI>AgCl>Ag2S
参考答案:C
本题解析:沉淀由AgCl AgI
AgI Ag2S,故溶解度AgCl>AgI>Ag2S。
Ag2S,故溶解度AgCl>AgI>Ag2S。
本题难度:简单