时间:2017-08-26 00:29:24
1、选择题 有甲、乙两种溶液,甲溶液的pH是乙溶液pH的2倍,则甲、乙两溶液中的C(H+)
A ?2:1? B 100:1 ?C? 1:100?D ?无法确定
参考答案:D
本题解析:略
本题难度:一般
2、填空题 以下各题中各量的关系,请用“﹥”、“=”或“﹤”表示。
(1)pH = 3的醋酸和pH=11的氢氧化钠溶液等体积混合,混合液中c(Na+) ?c(CH3COO-)
(2)等物质的量浓度、等体积盐酸和醋酸钠混合,混合液中各离子浓度的大小关系为?
?
(3)常温下,若NaOH溶液中的c(OH-)与NH4Cl溶液中的c(H+)相同。现将NaOH和NH4Cl的溶液分别稀释10倍,稀释后NaOH和NH4Cl溶液的pH分别用pH1和pH2表示。则pH1+ pH2??14
(4)现有pH相等、等体积的Ba(OH)2、NaOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合,混合后溶液均呈中性,则V1 、V2 、V3的大小关系?
参考答案:(1)c(Na+)﹤? c(CH3COO-)(2) c(Cl-)=c(Na+)﹥c(H+)﹥c(CH3COO-)﹥c(OH-)?
(3)pH1+ pH2?﹤? 14 (4)V1、V2、V3的大小关系? V3﹥ V1 =V2
本题解析:(1)pH相同的弱酸与强碱等体积混合,溶液最终显酸性,c(H+)> c(OH—),由电荷守恒知另两离子浓度必然是:c(Na+)﹤?c(CH3COO-)
(2)等物质的量浓度、等体积盐酸和醋酸钠混合后即是等浓度的NaCl和CH3COOH溶液,NaCl全部电离,CH3COOH部分电离,溶液显酸性。
即:c(Cl-)=c(Na+)﹥c(H+)﹥c(CH3COO-)﹥c(OH-)
(3)可以用假设法更直接。假设NaOH溶液的pH为11、NH4Cl溶液的pH则为3,
如果同时稀释10倍,则NaOH溶液的pH为12,而NH4Cl溶液由于有水解平衡的存在,其pH则就略小于4,故pH1+ pH2?﹤?14
(4)两强碱溶液中OH—浓度相同,必然消耗相同的酸,故V1 =V2,?而弱碱里面存有电离平衡,必然要消耗更多的酸,所以V3﹥ V1 =V2
本题难度:一般
3、选择题 25℃时,amol.L-1一元酸HA与bmol.L-1NaOH等体积混合后,pH为7,则下列关系一定正确的是
A.a =b
B.a>b
C.c(A-) = c(Na+)
D.c(A-)<c(Na+)
参考答案:C
本题解析:若HA为强酸,a=b;若HA为弱酸,则a>b,但无论HA是强酸还是弱酸,均有电荷守恒:
c(Na+)+ c(H+)=c(A-)+ c(OH—),pH=7,c(H+)= c(OH—),所以c(A-) = c(Na+)。
点评:本题可直接根据电荷守恒解答。
本题难度:一般
4、选择题 下列热化学方程式中ΔH代表燃烧热的是
A.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH1
B.S(s)+3/2O2(g)=SO3(s)ΔH2
C.CH4(g)+3/2O2(g)=2H2O(l)+CO(g)ΔH 3
D.2CO(g)+O2(g)=CO2(g)ΔH4
参考答案:A
本题解析:燃烧热:25℃、101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,A、符合燃烧热的定义,正确;B、S不能直接一步生成SO3,错误;C、应生成CO2不应是CO,错误;D、燃料系数不是1mol,错误。
考点:考查燃烧热的定义。
本题难度:一般
5、选择题 下列四组溶液的pH前者大于后者的是:
A.物质的量浓度相同的盐酸和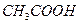 溶液
溶液
B.物质的量浓度相同的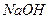 溶液和氨水
溶液和氨水
C.pH=3的盐酸和pH=3的 溶液均稀释100倍所得溶液
溶液均稀释100倍所得溶液
D.pH=10的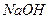 溶液和pH=10的
溶液和pH=10的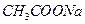 溶液均稀释100倍所得溶液
溶液均稀释100倍所得溶液
参考答案:BC
本题解析:略
本题难度:简单