时间:2017-08-26 00:22:03
1、选择题 下列电离方程式正确的是(?)
A.H3PO4 3H++
3H++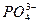
B.CaCO3 Ca2++
Ca2++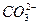
C.NaHS Na++H++S2-
Na++H++S2-
D.2H2O H3O++OH-
H3O++OH-
2、填空题 (6分)根据下列事实,完成相关的离子方程式或电离方程式
(1)Na2S溶液使酚酞显红色
(2)硫酸铝钾[明矾KAl(SO4)2・12H2O]可以作净水剂
(3)常温下,磷酸(H3PO4)溶液pH
3、填空题 某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-;HB-?H++B2-。回答下列问题。
(1)Na2B溶液显________(填“酸性”、“中性”或“碱性”),理由是________________(用离子方程式表示)。
(2)在0.1 mol・L-1的Na2B溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol・L-1
B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
D.c(Na+)=2c(B2-)+2c(HB-)
(3)已知0.1 mol・L-1 NaHB溶液的pH=2,则0.1 mol・L-1 H2B溶液中的氢离子的物质的量浓度可能________0.11 mol・L-1(填“<”、“>”或“=”),理由是_________________________________________________________________。
(4)0.1 mol・L-1 NaHB溶液中各种离子浓度由大到小的顺序是_____________。
4、选择题 将0.1 mol・L-1的氨水加水稀释至0.01 mol・L-1,稀释过程中温度不变,下列叙述正确的是( )
A.稀释后溶液中c(H+)和c(OH-)均减小
B.稀释后溶液中c(OH-)变为稀释前的1/10
C.稀释过程中氨水的电离平衡向左移动
D.稀释过程中溶液中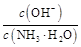 增大
增大
5、选择题 已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2mol・L-1HF溶液中加入1 L 0.2 mol・L-1CaCl2溶液,则下列说法中,正确的是(?)
A.25℃时,0.1 mol・L-1HF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中有CaF2沉淀产生
D.加入CaCl2溶液后体系中的c(H+)浓度不变