ʱ��:2017-08-22 17:08:22
1��ѡ���� ��A��B��C��D�Ŀ��������A��B�õ�����������������������Һ�У�B����ʴ����A��D�ֱ�Ͷ���Ũ�������У�D��A��Ӧ���ҡ���ͭ����B������Һ������Ա仯�������ͭ����C������Һ��н���C�������ݴ��ж����ǵĻ����ǿ������˳���ǣ�?��?
A��D >C >A >B?B. D >A >B >C
C��D >B >A >C?D��B >A >D >C
�ο��𰸣�B
���������ԭ����б���ʴ�Ľ����ǻ��ǿ�Ľ�������������ͬ���ᷴӦʱ�����ǿ�Ľ�����Ӧ���ң��������û���Ӧ�У��ϻ��ý������û����ϲ����õĽ������ݴ˿��Խ�����ֻ�Բ�ͬ�Ľ����͵������Һ����ԭ��أ��ϻ��õĽ����������������Ͻ���ʧ���ӷ���������Ӧ����ʴ���ϲ����õĽ�������������A��B�õ���������������������Һ�У�B����ʴ������A�Ļ�Դ���B����������ͬ���ᷴӦʱ�����ǿ�Ľ�����Ӧ���ң���A��D�ֱ�Ͷ���Ũ��������Һ�У�D��A��Ӧ���ң�����D�Ļ�Դ���A���������û���Ӧ�У��ϻ��ý������û����ϲ����õĽ�������ͭ����B������Һ�У������Ա仯��˵��B�Ļ�Դ���ͭ�������ͭ����C������Һ�У��н���C������˵��ͭ�Ļ�Դ���C�����Խ����Ļ��˳��Ϊ��D��A��B��C����ѡB��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣����������ѧ���������������ͷ�ɢ˼ά����������ʱ�ܴ�ԭ��صĸ���������֮����û���Ӧ�����������ˮ��Ӧ�ľ��ҳ̶ȡ���������������ˮ����ļ���ǿ���ȷ������жϽ����Ļ��ǿ����ע�����֪ʶ�Ļ��ۺ��ܽᡣ
�����Ѷȣ���
2��ѡ���� ����п��ͭ��ϡ������ɵ�ԭ��أ���ͼ���������й�˵����ȷ���ǣ�������
A��Zn�Ǹ���
B��������Zn�����·����Cu
C��Zn�缫�Ϸ�����ԭ��Ӧ
D��Cu�缫��Ӧ��Cu2++2e-�TCu
�ο��𰸣�A��Zn��Cu�����ṹ�ɵ�ԭ����У����ý���п������������ͭ����������A��ȷ��
B��ԭ����е�������������������ͭƬ����������пƬ����B����
C��ԭ��صĸ�����Ӧ�Ǹ�������ʧ���ӵ�������Ӧ����C����
D��ԭ��ص�������Ӧ�ǣ�2H++2e-��H2������D����
��ѡA��
���������
�����Ѷȣ���
3������� ��5�֣���ͼA��B��C�����ձ��зֱ�ʢ����ͬ���ʵ���Ũ�ȵ�ϡ���ᡣ
��1��A�з�Ӧ�����ӷ���ʽ��_______________________________________��
��2��B��Cu���ĵ缫��Ӧʽ��______________________________________��
��3��C�б���ʴ�Ľ�����__________���ѧʽ����A��B��C��������ʴ�����ʣ��ɿ쵽������˳����_____________���á�������ʾ����
�ο��𰸣�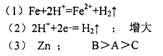
�����������
�����Ѷȣ���
4��ѡ���� ��ͼ��п-ͭ-ϡ����ԭ���װ�ã�����������ȷ�ĵ���
A��п��������ͭ�Ǹ����������ķ����Ǵ�п��ͭ
B��пƬ�������٣�ͭƬ��������
C�����������Ϸ����Ķ���������ԭ��Ӧ
D��ԭ����е������仯�ǣ���ѧ��ת��Ϊ����
�ο��𰸣�D
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ��п�Ľ�����ǿ��ͭ�ģ�����п�Ǹ�����ʧȥ���ӡ�ͭ����������Һ�е��������������õ����ӣ�����������������A��B��C������ȷ��D��ȷ����ѡD��
�������������е��Ѷȵ����⣬���������ǿ������������ѧ���������������ͷ�ɢ˼ά����������Ĺؼ�����ȷԭ��ع���ԭ����Ȼ��������������ü��ɣ����������ѧ����Ӧ������������ѧ����ѧ��������
�����Ѷȣ�һ��
5��ѡ���� ������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�
A�������£���0.01mol��L��NH4HSO4��Һ�еμ�NaOH ��Һ�����ԣ�
c(Na��)>c((SO42��)>c(NH4��)>c(OH��)��c(H��)
B��0.1mol��L��1NaHCO3��Һ��c(Na��)>c(OH��)>c((HCO3��)>c(H��)
C��Na2CO3��Һ��c(OH��)��c(H��)��c((HCO3��)+2c(H2CO3)
D��25��ʱ����pH��4.75��Ũ�Ⱦ�Ϊ0.1mol��L��1��CH3COOH ��CH3COONa �����Һ��
c(CH3COO��)��c(OH��)<c(CH3COOH)��c(H��)
�ο��𰸣�AC
�������������HCO3����ˮ��Ͼ������ģ�����c(OH��)�����ܴ���c((HCO3��)������B����
D�еĹ�ϵӦ�ǣ�c(CH3COO��)��c(OH��)��c(CH3COOH)��c(H��)������D����
��ȷ��ΪA��C��
�����Ѷȣ�һ��