时间:2017-08-22 15:04:43
1、选择题 如图所示,6个编号分别表示六种物质:Al、Fe2O3、NaOH溶液、氢碘酸、NH3、O2。凡是直线相连的两种物质均能发生化学反应(已知高温时氨气能还原Fe2O3。)图中①表示的物质是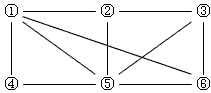
[? ]
A.Al
B.NaOH溶液
C.氢碘酸
D.O2或Fe2O3
2、填空题 金属单质A与盐酸反应生成浅绿色溶液B,同时放出气体C。如果在B溶液中通入氯气,则B转变成棕黄色溶液D,将溶液D分为两份,一份加入几滴KSCN溶液,溶液变成血红色,另一份加入A,则棕黄色溶液D重新变成浅绿色溶液B。则:
(1)各物质的化学式分别是:A________ ,B________ ,C________ ,D________;
(2)有关反应的离子方程式有:
① B→D___________________________;
② D→B____________________________。
3、推断题 (15分)
某学习小组利用某工业废弃固体(主要成分为Cu2S和Fe2O3)来研究相关物质的制备。设计方案如图所示: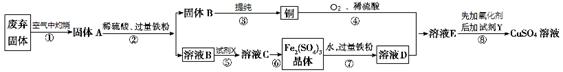
已知:Ksp[Cu(OH)2]=6.0×10-20 ,Ksp[Fe(OH)2]=1.6×10-14 ,Ksp[Fe(OH)3]=1.0×10-38
(1) 废弃固体在空气中灼烧发生反应(有2种元素被氧化)的化学方程式为______。
(2) 溶液C通过_______、_________、过滤等操作得到Fe2(SO4)3晶体。
(3) 常温下,铜粉、O2和稀硫酸三者在一起生成硫酸铜反应极慢。当往其中加入溶液D后,随即生成硫酸铜。这一过程中反应的化学方程式依次为4FeSO4 + O2 + 2H2SO4=2Fe2(SO4)3?+ 2H2O和?。溶液D在这一过程中所起的作用是_______。
(4) 操作⑧的目的是制取较纯的硫酸铜溶液。溶液E中加入试剂Y以调节pH使得铁元素全部形成沉淀(含铁元素的离子浓度小于10-5 mol・L-1)。试剂Y可以是??,溶液的pH至少调节为________。
4、填空题 某不锈钢(主要成分为Fe)样品中含有铝、铜等(其它成分忽略),为了测定该合金中铁的含量,有人设计如下工艺流程: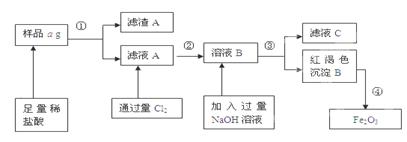
(1)滤液C中溶质含有_? _(写化学式);
(2)如何验证滤液A中含Fe2+,而不含Fe3+____?_____。
(3)对所得Fe2O3固体称量得质量为b g,计算该样品中铁元素质量分数的表达式为(用含a、b的式子表示)___?__。
5、选择题 在Fe2(SO4)3溶液中,加入a g铜,完全溶解后,再加b g铁,充分反应后得到c g残余固体,且a>c,则下列说法正确的是(? )
A.残余固体是铜和铁
B.最后得到的溶液中一定含有Cu2+
C.将残余固体加入到稀硫酸中,有气泡产生
D.最后得到的溶液中可能含有Fe3+