时间:2017-08-22 14:05:07
1、填空题 在室温下,下列五种溶液①0.1mol/LNH4Cl ②0.1mol/LCH3COONH4 ③ 0.1mol/ L NH4HSO4 ④0.1mol/LNH3・H2O和0.1mol/LNH4Cl的混合溶液 ⑤0.1mol/LNH
0.1mol/ L NH4HSO4 ④0.1mol/LNH3・H2O和0.1mol/LNH4Cl的混合溶液 ⑤0.1mol/LNH 3・H2O
3・H2O
(1)溶液①呈___性(填“酸”“碱”或“中”)其原因是____________________________(用离子方程式表示)
(2 )比较溶液②、③中C(NH4+)的大小关系是____________________(填>,<或=)
)比较溶液②、③中C(NH4+)的大小关系是____________________(填>,<或=)
(3)在溶液④中,_____________离子的浓度为0.1mol/L
NH3・H2O和_________离子的物质的量浓度之和为0.2mol/L
(4) 室温下测得溶液②的PH=7,则说明CH3COO-的水解程度_______(填>,<或=")" NH4+的水解程度,C(CH3COO-)_________C(NH4+)(填>,<或=)
2、选择题 25℃时,向10ml0.01mol/LKOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的
A.pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-)
B.pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-)
C.V[C6H5OH(aq)]=10ml时,c(K+)=c(C6H5O-)>c(OH-)=c(H+)
D.V[C6H5OH(aq)]=20ml时,c(C6H5O-)+c(C6H5OH)=2c(K+)
3、选择题 下列溶液中各微粒的浓度关系或说法正确的是
A.0.1 mol・L-1pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
B.等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3・H2O;c(NH4+)由大到小的顺序是:①>②>③>④
C.a mol・L-1HCN溶液与b mol・L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b
D.0.1 mol・L-1的醋酸的pH=a,0.01 mol・L-1的醋酸的pH=b,则a+1=b
4、填空题 (1)常温下有PH分别为8、9、10的三种相同物质的量浓度的盐溶液NaX、NaY、NaZ,比较盐酸、HX、HY、HZ四种酸酸性由强到弱
(2)已知25°C时: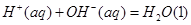
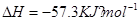
氢氟酸是一种弱酸,可用来刻蚀玻璃。20ml0.1mol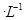 的氢氟酸与0.1mol/L
的氢氟酸与0.1mol/L
氢氧化钠溶液完全反应时放热aJ,写出氢氟酸电离的热化学方程式
5、选择题 下列离子方程式中,属于水解反应的是