时间:2017-08-10 02:33:40
1、实验题 ( 16分)某兴趣小组拟利用如下图装置探究验证干燥的Cl2和潮湿的C l2有无漂白性。
l2有无漂白性。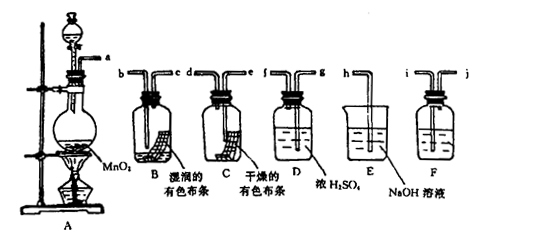
回答下列问题:
(1)A装置中的主要玻璃仪器有:导管、酒精灯、圆底烧瓶、?。
A装置中发生反应的化学方程式是?。
F装置中的试剂应为?,作用为?。
(2)按气体从左向右流向将各装置依次连接起来(填接口标号): a?接?,
?接?,?接?,?接?,?接 ?。
?。
(3)通入Cl2后,从集气瓶A、B中 红色布条的现象可得出的结论是?
红色布条的现象可得出的结论是?
?;其中发生的反应的化学方程式为?。
(4)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是?
?。
(5)烧杯E中发生反应的化学方程式为?。
(6)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛4 mol·L-1的NaOH溶液的体积至少应为?mL。
2、实验题 (14分)某化学兴趣小组为探究铜与浓硫酸的反应,用下图所示装置进行有关实验。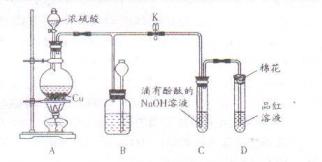
(1)装置D中试管口放置的棉花中应浸一种液体,这种液体是?,其作用是?。
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是?。B中应放置的液体是?(填字母)。
a.水 b.酸性KMnO4?c.浓溴水? d.饱和NaHSO3
(3)取6.4g铜片和12mL 18.4mol·L-1浓硫酸放在圆底烧瓶中共热, 直到反应完毕,最后发现烧瓶中还有铜片剩余。某同学根据所学的化学知识认为还有一定量的硫酸剩余。
直到反应完毕,最后发现烧瓶中还有铜片剩余。某同学根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是?
②下列药品能用来证明反应结束后烧瓶中确实有余酸的是?(填字母)。
a.铁粉? b.银粉? c.碳酸氢钠溶液? d.氯化钡溶液
(4)为定量测定余酸物质的量浓度,某同学进行了如下设计:先测定铜片和浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度。测定SO2的量的方案很多,下列方案可行的是
?(填字母)
a.将装置中产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量
b.将装置中产生的气体缓缓通入足量氢氧化钡溶液中,反应完全后过滤、洗涤、干燥、称量沉淀
c.将装置中产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液中,反应完全后过滤,洗涤干燥、称量沉淀
3、简答题
工业上常用铁质容器盛装冷浓硫酸,为研究铁质材料与热浓硫酸的反应,某学校学习小组进行以下探究实验:
[一](1)将已除去表面氧化物的铁钉(碳素钢)放入冷的热的浓硫酸中,10分钟后移人硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是??;
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用?
(选填序号)
a.KSCN溶液和氯水 .b铁.粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应SO2+Br2+2H2O═2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g由于此推知气体Y中SO2的体积分数为?;
[探究二]分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和Q气体,为此设计了下列探究实验装置(图中夹持仪器省略)
(3)装置B中试剂的作用是??;
(4)认为气体Y中还含有Q的理由是?;(用化学方程式表示)
(5)为确认Q的存在,需在装置中添加M于??(选填序号)
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验的现象应是?;
(7)若要测定限定体积气体Y中H2含量(标准状况下约有28ml H2),除用测量H2体积方法外,否选用质量称量方法?做出判断并说明理由??。
4、实验题 (9分)有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应。请回答下列问题:
(1)第一小组同学设计如图装置进行实验。通入SO2气体,将带余烬的木条插入试管C中,木条复燃。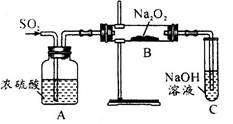
甲同学认为Na2O2与SO2反应生成了Na2SO3和O2,则反应的化学方程式为___________________________。
乙同学认为Na2O:与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成。为检验是否有Na2SO4生成,该同学设计了如下方案: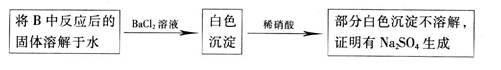
你认为乙同学的方案是否合理____________(答“是”或“否”);请简要说明两点理由:
①__________________________________________________________________________
②__________________________________________________________________________.
(2)第二小组同学利用下图中的有关装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应。已知:H2C2O4  ?CO2↑+CO↑+H2O
?CO2↑+CO↑+H2O
(乙二酸)?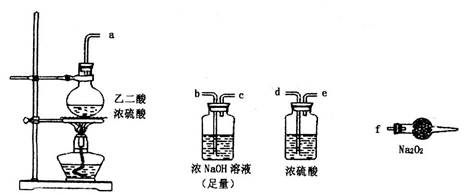
若CO能够与Na2O2发生反应,则预测反应产物为______________________;验证该产物可选择的试剂是___________________________________________________。
上述实验中选择的最简单的装置接口连接顺序为_________________________.
5、实验题 (12分)某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂。
【猜想与探究】猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物。
探究:过氧化钠与水反应的生成物的成分。
【实验与结论】
| ? | 实验操作 | 实验现象 | 实验结论 |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | ? _____________________ | 猜想a、c不成立,猜想b成立。 |
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有___________ |
| ②往①试管内的溶液中滴加___________ ______________ | ? _____________________ | 生成物有氢氧化钠 |
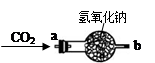
| 实验操作 | 实验现象 | 实验结论 |
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: ____________________________ |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |