ʱ��:2017-08-10 01:51:53
1��ѡ���� ��0��1mol��Ͷ�뵽�� 100mL3mol��L�ģ�NaOH��Һ�г�ַ�Ӧ���ٵ���lmol��L��H2SO4120mL������(? )
100mL3mol��L�ģ�NaOH��Һ�г�ַ�Ӧ���ٵ���lmol��L��H2SO4120mL������(? )
A����Һ��pH<7
B���õ���������Һ
C���������
D�����а�ɫ�������ɣ������ܽ�
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
2��ѡ���� ʮ���������ڣ����ļ۸�ʮ�ְ������������˵�ʱ�ƽ�ļ۸�������Ϊ��������
A�������Ʊ��Ƚ�����
B�����Ǻ��ȶ��Ľ���
C����Ԫ������Ȼ��ĺ�������
D��������;̫��
�ο��𰸣�A��ʮ���������ڣ�����������ȡ��û�к����ķ�������ȡ���Ѽ�֮���٣����¼۸���ߣ���A��ȷ��
B���������Ļ�ѧ���ʲ��ȶ������ڱ����γ�һ������Ĥ����B����
C������������Ȼ�����ŵ���λ���������٣���C����
D������������;�㲻����Լ�������۸���ԭ���������Ҷ࣬�������������Զ࣬�ؼ����Ʊ��Ƚ����ѣ���D����
��ѡA��
���������
�����Ѷȣ���
3��ѡ���� ��14�֣������������Ի������Һ�о�����NO3������������ԭ��Ӧ��ת����ϵ����ͼ��ʾ�� ��
��
���У�����D��F��Ӧ�������Σ�����D��A��Һ��Ӧ���ɰ�ɫ������
��ش��������⣺��
��1����Al��ϡ���ᷴӦʱ��ϡ������ֵ���������������������������
A��ֻ����ǿ������?
B��ֻ��������
C��ͬʱ����ǿ�����Լ�����
D��������ǿ�����Ի������˻�ԭ��
��2�����������ӷ���ʽ�ĺ�������д����Ļ�ѧʽ������Ҫ��ƽ��
������Al + NO3��+ OH��+ H2O��������������+����������
��3������D��ˮ��Һ��A��Һ��Ӧ�����ӷ���ʽ����������?��������
��4��D����C��Ӧ�Ļ�ѧ����ʽ��?
��5��C��E��������л���ɴ�����Ⱦ���ڴ��������£�D���Խ�C��Eת��Ϊ������̬���ʣ��õ�������������������
��6����ȥC�е�E�������ʿ��õĻ�ѧ�����ǣ����û�ѧ����ʽ��ʾ��?
��7��Al��NO3�������������·�Ӧ��Al�뱻��ԭ��NO3�������ʵ���֮��������?��������
�ο��𰸣�(16�֣�ÿС��2��)
��1����C��
��2����AlO2����+����NH3 ��
��3����3NH3��H2O��+ Al3+ ="=" Al(OH)3��+3 NH4+?��
��4��? 4 NH3 +5O2 ="=" 4NO + 6 H2O
��5����N2����
��6��? 3NO2 + H2O ="=" 2HNO3 + NO?
��7��? 1:1
���������
�����������Ի������Һ�о�����NO3������������ԭ��Ӧ������ͼʾ��Ϣ��֪�������Ի����£���Ӧ�������κ�һ�����������Ի���������ƫ�����κͰ�����������������������һ��������ˮ��һ���������Ժ�������Ӧ���ɶ�����������AΪ��������BΪƫ�����Σ�CΪNO��DΪ������EΪ����������FΪ���ᣮ
��1��Al��4HNO3=Al(NO3)3��NO����2H2O,HNO3�еĵ����ֱ�ۣ�ͬʱ����ǿ�����Լ����ԣ�ѡC���ʴ�Ϊ��C��
��2����ԭ���غ�͵�ʧ�����غ�ã���������������AlO2�D��ʽ���ڣ�������������������һ��������ˮ���ʴ�Ϊ����AlO2����+����NH3 ��
�ǹ����İ�ˮ�����ܽ�Al(OH)3����3NH3��H2O��+ Al3+ ="=" Al(OH)3��+3 NH4+������Ӧ��������������ɫ�������ʴ�Ϊ����3NH3��H2O��+ Al3+ ="=" Al(OH)3��+3 NH4+
��4��D����C��Ӧ�Ļ�ѧ����ʽ����������������һ��������ˮ4 NH3 +5O2 ="=" 4NO + 6 H2O�ʴ�Ϊ��4 NH3 +5O2 ="=" 4NO + 6 H2O
��5��6NO��4NH3=5N2��6H2O,8NH3��6NO2=5N2��12H2O��������ΪN2, �ʴ�Ϊ����N2��
�ʿ�����ˮϴ����3NO2 + H2O ="=" 2HNO3 + NO���ʴ�Ϊ��3NO2 + H2O ="=" 2HNO3 + NO
��Al��NO3�������������·�Ӧ��������������Ϊ���۵������ӣ�ʧȥ����3mol�����������ԭΪһ���������õ�����Ҳ��3mol�����ݵ����غ㣬Al�뱻��ԭ��NO3�������ʵ���֮����1��1���ʴ�Ϊ��1��1��
�����Ѷȣ�һ��
4��ѡ���� ���������У�������ǿ�ᷴӦ�����ܸ�ǿ�Ӧ���ǣ���������NaHCO3?��Al?��Al2O3?��Al��OH��3��
A���٢ڢ�
B���ڢۢ�
C���٢ۢ�
D���٢ڢۢ�
�ο��𰸣��١�NaHCO3�������������Σ��������ᷴӦ������CO2���壬������Ӧ�������Σ��ʢ���ȷ��
�ڡ����������ᷴӦ����Al3+����������Ӧ����AlO2-���������ʢ���ȷ��
�ۡ�Al2O3��������������������ᷴӦ������Al3+���ӣ�������Ӧ����AlO2-���ӣ��ʢ���ȷ��
�ܡ�Al��OH��3?����������������������ᷴӦ������Al3+���ӣ�������Ӧ����AlO2-���ӣ��ʢ���ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
5������� ��8�֣������й�����֪����������������Һ��Ӧʵ���Ƿ������������У�
��1����2Al+6H2O=2Al(OH)3+3H2��?��2����Al(OH)3+NaOH=Na[Al(OH)4]
�Իش��������⣺
��1����������������Һ��Ӧ�����ӷ���ʽΪ��?��
��2���ж�������Ӧ�ķ�Ӧ���ͣ������ֻ�����Ӧ��������
�ٵ�1����?���ڵ�2����?��
��3��������ķ�������������������Һ��Ӧ����������?��
��ԭ����___________��
��4������ Na[Al(OH)4] +4HCl = AlCl3 + NaCl + 4H2O ���������У���д����1���Ļ�ѧ����ʽ��
��1����?
��2����Al(OH)3 + 3HCl = AlCl3 + 3H2O
�ο��𰸣���1��2Al + 2OH- +6H2O = 2[Al(OH)4]- +3H2��?��2�֣�
��2���û���Ӧ��1�֣�?���Ϸ�Ӧ��1�֣� ?��3��H2O��1�֣�? Al ��1�֣�?
��4��Na[Al(OH)4] + HCl =" NaCl" +Al(OH)3��+ H2O��2�֣�
�����������1����+��*2�ͻ���ȥAl(OH)3���õ���������������Һ��Ӧ�ķ���ʽ��
��3��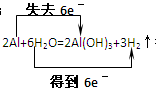 �õ���������������Һ��Ӧ����������H2O����ԭ��ΪAl��
�õ���������������Һ��Ӧ����������H2O����ԭ��ΪAl��
��4���ܷ�Ӧ����ʽ��ȥ�ڶ�����ѧ����ʽ���ͻ�õ���һ����ѧ����ʽ��Na[Al(OH)4] + HCl =" NaCl" +Al(OH)3��+ H2O��
�����Ѷȣ�һ��