ʱ��:2017-08-10 01:51:53
1��ѡ���� �����йؽ�������Ͻ��˵������ȷ���ǣ�������
A��Ŀǰ�ҹ���ͨ��Ӳ�����ɺϽ���������
B����������ͨ�ֵIJ�����е�̼������������
C��þ�ڿ�����ȼ�շ���ҫ�۵İ⣬����������������
D����������Ʒ���渲��������Ĥ�����ڲ������𱣻�����
�ο��𰸣�A��Ŀǰ�ҹ���ͨ��Ӳ�����ɺϽ�����Ƴɣ�1�ǵ�Ϊ����֣�5�ǵ�Ϊ��о��ͭ��1Ԫ��Ϊ��о��������Aѡ����ȷ��
B��������̼����ߣ���ͨ�ִ�֮����������٣���Ŀ˵������ʵ�෴����Bѡ��˵������
C����������������������þȼ�շ���ҫ�۵İ⣬��Cѡ����ȷ��
D�������渲�����ܵ������ﱡĤ���Խ����𱣻����ã���Dѡ����ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
2�������� ��15�֣�ijͬѧ�ԡ����ȷ�Ӧ��������������������������Ӧ�ų��������ȣ����ų�ҫ�۵Ĺ�â������ֽ©�����²����մ���������������ɳ�С����ɻ�ѧ�ֲ���ĵ��й����ʵ��ۡ��е��������±���
| ���� | Al | Al2O3 | Fe | Fe2O3 |
| �۵�/�� | 660 | 2054 | 1535 | 1462 |
| �е�/�� | 2467 | 2980 | 2750 | ? |
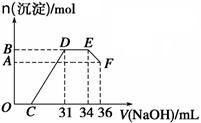
�ο��𰸣���.��1��������1�֣���
��2��NaOH��Һ��2�֣���2Al��2OH����2H2O===2AlO��3H2����2�֣�
��.��1�� H����OH��===H2O��2�֣�
��2��NH��OH��===NH3��H2O��NH��OH��===NH3��+H2O��2�֣�
��3��H+ �� Fe3+ �� Al3+ �� NH��2�֣�
��4��0.008��2�֣�
��5��0.032��1�֣���7��1�֣�
������������ȷ�Ӧ2Al+Fe2O3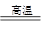 2Fe+Al2O3?2Al��2OH����2H2O===2AlO��3H2��
2Fe+Al2O3?2Al��2OH����2H2O===2AlO��3H2��
��ͼ��֪OC������кͣ�����31ml�ļ�����������ij�����34---36ml���ɵ�����������ǿ���ܽ⡣
Al(OH)3+OH��=AlO+2H2O
4 mol��L��1��4ml
�����Ѷȣ�һ��
3������� ��14�֣�þ������������Ҫ�Ľ��������ǵĵ��ʼ����������Ÿ��Ե����ʡ�
��ˮ�к����Ȼ�þ����þ����Ҫ��Դ֮һ���Ӻ�ˮ����ȡþ��ijͬѧ���������
���̲��裺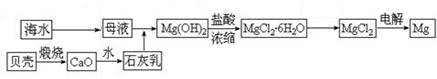
��Ҫ�IJ����ܽ����£��ٰѱ����Ƴ�ʯ����?����ĸҺ�м�ʯ���飬���������ˣ��õ�Mg(OH)2����?�۽������������ᷴӦ���ᾧ�����ˣ����Ƶõľ�����ˮ����ˮMgCl2
�ܽ��õ��IJ������ں��⡣
��1������˵������ȷ����__________________������ţ�
A���˷����ŵ�֮һ��ԭ����Դ�ḻ
B�����Т٢ڢ۲����Ŀ���ǴӺ�ˮ����ȡ�Ȼ�þ
C���ڢܲ���ⷨ��ȡþ������þ�Ǻܻ��õĽ���
D��������ȡþ�Ĺ������漰�ķ�Ӧ�зֽⷴӦ�����Ϸ�Ӧ���û���Ӧ
��2������ڲ���������������?
��1��������������ˮ�����һ�ֵ�أ��㷺�������캽��ơ��˵�������ĵ缫��ӦΪ?��
��2�����Ȼ�ԭ����ұ���۵�ϸߵĽ�����һ����Ҫ���������Ӹֹ켴�õ��˷������������������ĩ�����۾��Ȼ�Ϻ����ֽ©���У�©�������ȴ����ã�������������̨�ϣ�
�������һ��ʢ��ɳ�ӵ���������д���������ȷ�Ӧ�IJ������÷�Ӧ�Ļ�ѧ����ʽ��
����?
��ѧ����ʽ?��
��3��Ϊȷ��ij���ȼ�����������ĩ�����ۣ�����ɣ��ֱ��������ʵ�顣
��ȡ10.7g��Ʒ�������м���������NaOH��Һ��������ɵ����壨��״�������Ϊ3.36L����Ӧ�Ļ�ѧ����ʽΪ?����Ʒ������������?g��
��ȡ10.7g��Ʒ�����ȼ��ǡ����ȫ��Ӧ������Ӧ������ȴ�����������ᣬ������ɵ��������ΪaL������������С�����������������ȵ���?��?��
�ο��𰸣���14�֣���1��D ��1�֣�
��2��ʯ�����е�Ca(OH)2Ϊ����Ƶõ�Mg(OH)2����������1�֣�
��1����1��O2 + 4e��+2H2O?4OH����2�֣�
��2���ڻ�������������������ع��壬�м����һ����ɰֽ��ĥ����þ������ȼþ������2�֣�? 2Al+Fe2O3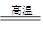 Al2O3+2Fe ��2�֣�
Al2O3+2Fe ��2�֣�
��3��2Al+2NaOH+2H2O==2NaAlO2+3H2�� ��2�֣�? 2.7 ��2�֣�? 2:3 ��2��
�����������1���ѱ����Ƴ�ʯ�����漰������Ӧ�����ȱ��Ǹ��·ֽ��Ƴ������ƣ�Ȼ����������ˮ����Ƴ�ʯ���飻������ĺ�ˮ�м�ʯ�����ʯ�������Ҫ�ɷ����������뺣ˮ�е�þ���ӽ������������þ������������þ�����ᷴӦ�����Ȼ�þ��������ڵ��Ȼ�þ�õ�����þ����������ת�����̣���֪��Ӧ��û���漰�û���Ӧ��D����ȷ������ѡ�����ȷ�ģ���ѡD��
��2������ʯ�����е�Ca(OH)2Ϊ��������Ƶõ�Mg(OH)2����������˲���ڲ���������
��1�����ǻ��õĽ�����������������������ͨ�룬���������缫��Ӧʽ��O2 + 4e��+2H2O?4OH����
��2�����ȷ�Ӧ����ȷ�����ǣ��ڻ�������������������ع��壬�м����һ����ɰֽ��ĥ����þ������ȼþ������Ӧ�Ļ�ѧ����ʽ��2Al+Fe2O3 Al2O3+2Fe��
Al2O3+2Fe��
��3�����ȼ��к�����������Һ��Ӧ���ǵ���Al�����Է�Ӧ�Ļ�ѧ����ʽ��
2Al+2NaOH+2H2O��2NaAlO2+3H2�������������ʵ�����3.36L��22.4L/mol��0.15mol����˸��ݷ���ʽ��֪��Al�����ʵ�����0.1mol��������2.7g���������ȷ�Ӧ�����ɵ����������ʵ�����0.1mol��������ٺ��ᷴӦ���ɵ�������0.1mol�������������������ȵ���2�U3��
�����������ȷ�Ӧ���йؼ����У�Ӧ�����õ��ӵĵ�ʧ�غ�����йؼ��㣬���ڸ����У���������ϡ���ᷴӦʧȥ2�����ӣ�������3�����ӣ��������ֱ�����õ��ӵ�ʧ�غ�������ó�1�U1�Ĵ�����ۡ�����ھ���ļ����У�����Ҫ����������������������á�
�����Ѷȣ�һ��
4��ѡ���� �����йؽ������仯�����˵���������
A������ˮ�����ڸ��������·�Ӧ��������������������
B��ϡ�����м���ͭ�۲���Ӧ���ټ����������Բ���Ӧ
C��AlCl3��FeCl2��CuCl2����ͨ�����Ϸ�Ӧ�Ƶ�
D������̼������Һ��ͨ������������̼����Һ�����
�ο��𰸣�B
���������A������ˮ�����ڸ��������·� Ӧ������������������������ȷ��B��ϡ�����м���ͭ�۲���Ӧ���ټ��������Ʒ����ķ�ӦΪ��3Cu + 2NO3- + 8H+ ="===" 3Cu2+ + 2NO��+ 4H2O������C��AlCl3��CuCl2����ͨ�����������������Ƶã�FeCl2��ͨ�������Ȼ�����Һ�����Ƶã���ȷ��D������̼������Һ��ͨ������������̼������̼�����ƣ�̼�����Ƶ��ܽ��С��̼���ƣ���Һ����ǣ���ȷ��
�����Ѷȣ�һ��
5��ʵ���� ij�о���ѧϰС���ò�����������������ΪFe2O3��Ϊԭ�ϣ������ұ���������¹������̣����ַ�Ӧ����û�б������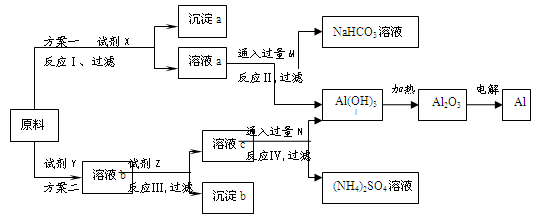
��1���Լ�X�Ļ�ѧʽΪ?����Ӧ������ӷ���ʽ��?��ʵ��������480mL 1 mol��L-1 X����Һ�����õ������������ձ������������Լ�ƿ����ͷ�ι��⣬����?�����������Ա궨����X����ҺŨ���Ƿ�ȷ��ʵ��������?��
��2�����շ�����ƣ��Լ�Z�������ǵ�����Һ��pH�������ɳ���b[Fe(OH)3]�����Լ���ҵ�ĽǶȣ�����Ϊ����?��������������?��
��3����֪NΪ������ʵ�����л���������ͼװ����ȡ���������а�����Ȫʵ�顣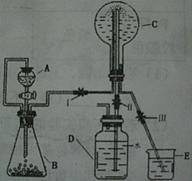
������A��������?��װ����A�ڲ���B�ڲ�֮����ͨ�����ܵ�������?��
�����ô�װ���Ʊ�N������A��ʢ��Ũ��ˮ����Bװ���еĹ����Լ�������ѡ�����е�?������ĸ��ţ���
a����ʯ��? b���ռ�? c������? d����ʯ��
��4�������£���a mol��L-1��(NH4)2SO4ˮ��Һ��pH=5��������ƽ��NH4++H2O  NH3��H2O+H+�����ƽ�ⳣ���ı���ʽΪ?���ú�����a�Ľ�Ϊ��ȷ�����ֱ���ʽ��ʾ�����ػ������������㣩��
NH3��H2O+H+�����ƽ�ⳣ���ı���ʽΪ?���ú�����a�Ľ�Ϊ��ȷ�����ֱ���ʽ��ʾ�����ػ������������㣩��
�ο��𰸣�
��1��NaOH��1�֣���Al2O3+2OH-+3H2O=2[Al(OH)4]-��2�֣���500mL����ƿ��2�֣���д500mLֻ��1�֣����ζ����к͵ζ���1�֣���
��2������һ��1�֣��������٣��ϼ�2�֣���
��3���ٳ���©����1�֣���ƽ������ѹǿ����ֹ����©��������2�֣���
��4��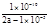 ��2�֣���
��2�֣���
���������
��1������ͼ�е�ԭ��Ϊ��������������ΪFe2O3��������I��Ϊ�ȼ���ǿ����Һ���˺�������Һ��ͨ�������̼���壬���õ����������ٽ��к������裻�ʴ��Լ�Xһ��ѡ��NaOH����ӦIΪ��Al2O3+2OH-+3H2O=2[Al(OH)4]-������480mL 1 mol��L-1����������Һʱ��Ӧѡȡ500mL����ƿ�ұ����������ƿ���ݻ���ȷ��������Һ��Ũ���Ƿ�ȷ��Ӧ���еζ����к͵ζ�ʵ�飻
��2���������У����ȼ��������ܽ��������������������ڲ�����м����Լ�����pHֵ���������������������˺�������������Һ��ͨ�백������ȡ���������������������������Է���һ�����٣��ϼ��ǽϼѷ�����
��3������װ��ͼ����ȡ�����������Ȫʵ��ʱ������AΪ����©����A�ڲ���B�ڲ�֮����ͨ�����ܵ�������ƽ������ѹǿ����ֹ����©��������
��4��a mol��L-1��(NH4)2SO4ˮ��Һ��pH=5������Һ�е�c(H+)=10-9mol��L-1����c(NH3��H2O)=c(OH-)=10-5mol��L-1��c(NH4+)=2a-10-5mol��L-1������ˮ������ӷ���ʽ��NH4++H2O  NH3��H2O+H+���ɵ�k=
NH3��H2O+H+���ɵ�k=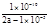 ��
��
�����Ѷȣ�һ��