ʱ��:2017-08-10 00:16:07
1��ѡ���� ���б仯���ڻ�ѧ�仯����?
A�����˳�ȥˮ�е���ɳ
B��ʳ�︯��
C��������ƾ���ˮ
D����Һ���������Ȼ�̼��ˮ
2������� һ�ֺ�����ﮡ��ܵ����͵��Ӳ��ϣ������в����ķ��������ɹۣ������е����Խ�����������ʽ���ڣ�����Co2O3?CoO����ʽ���ڣ������������ĵ����˫�棻﮻��������У��ӷ����л��������ܣ�CoO���Ĺ���������ͼ1��ʾ��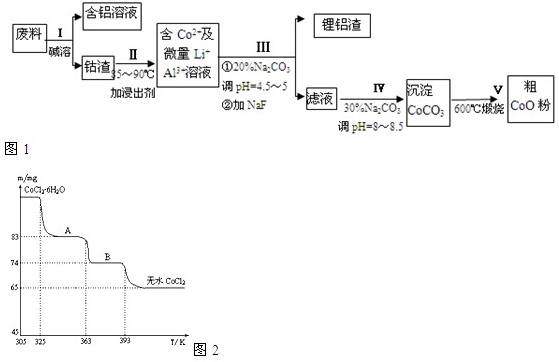
��1�����̢��в���NaOH��Һ�ܳ������е�Al����Ӧ�����ӷ���ʽΪ______��
��2�����̢��м���ϡH2SO4�ữ���ټ���Na2S2O3��Һ�����ܣ�������ܵĻ�ѧ��Ӧ����ʽΪ��������ֻ��һ�������______����ʵ����ģ�ҵ����ʱ��Ҳ������������ܣ���ʵ�ʹ�ҵ�����в������ᣬ��ӷ�Ӧԭ������������������ܵ���Ҫԭ��______��
��3�����̢�õ����������Ҫ�ɷ���LiF��Al��OH��3��̼������Һ�ڲ���Al��OH��3ʱ����Ҫ���ã���д���÷�Ӧ�����ӷ���ʽ______��
��4��̼������Һ�ڹ��̢�͢�����������������ͬ����д���ڹ��̢������������______��
��5����Na2CO3��Һ�д��ڶ������ӣ����и�����Ũ�ȹ�ϵ��ȷ����______������ţ���
A��c��Na+��=2c��CO32-��
B��c��Na+����c��CO32-����c��HCO3-��
C��c��OH-����c��HCO3-����c��H+��
D��c��OH-��-c��H+���Tc��HCO3-��+2c��H2CO3��
��6��CoO��������ɵ÷ۺ�ɫ��CoCl2��Һ��CoCl2���ᾧˮ��Ŀ��ͬ�����ֲ�ͬ��ɫ��������ɫ����ˮCoCl2��ˮ��ɫ��һ���ʿ��Ƴɱ�ɫˮ�������īˮ����ͼ�Ƿۺ�ɫ��CoCl2?6H2O�������ȷֽ�ʱ��ʣ������������¶ȱ仯�����ߣ�A���ʵĻ�ѧʽ��______��
3������� ±�����Ҫ�ɷ���MgCl2������� Fe3+��Fe2+��Mn2+�����ӡ���±��Ϊԭ�Ͽ��Ƶ���������þ��������������ͼ��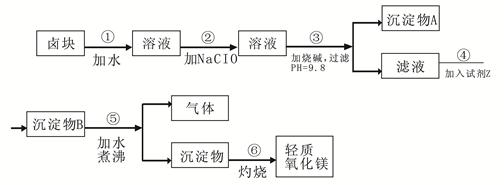
��֪��Fe2+�����������״�����״���Һ�г�ȥ�����Գ���������ΪFe3+������Fe(OH)3������ȥ����Ҫ���Ʒ�����������ʣ�����ݱ�1��2�ṩ�����ϣ���д�հף�?
��1?�����������������pH
| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��3 | 2.7 | 3.7 |
| Fe��OH��2 | 7.6 | 9.6 |
| Mn��OH��2 | 8.3 | 9.8 |
| Mg��OH��2 | 9.6 | 11.1 |
| �Լ� | �۸�Ԫ/�֣� |
| ƯҺ����NaClO��25.2%�� | 450 |
| ˫��ˮ����H2O2 ,30%�� | 2400 |
| �ռ��98% NaOH�� | 2100 |
| �����99.5% Na2CO3�� | 600 |
4������� ��13�֣���һ��ɫ��Һ�����ܺ���Fe3+��Al3+��Fe2+��Mg2+��Cu2+��NH4+��K+��CO32-��SO42-�����ӵļ��֣�Ϊ������ɷ֣�ȡ����Һ�ֱ�������ĸ�ʵ�飬��������й���������ͼ��ʾ��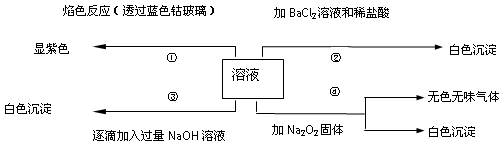 ?
?
�ڵڢ۸�ʵ���У����ɰ�ɫ�������������NaOH��������ͼ��ʾ�����ϵ���ݴ˿�֪��
����ԭ��Һ��һ�������ڵ�������_____________________��
��Ϊ�������Һ��һ�����ڵ����ӵ�Ҫ��һ����ܽ���
�ֳ�������Ϊ��д��ѧʽ��___________��_________��
��д���ڢ۸�ʵ���з�����Ӧ�����ӷ���ʽ
?��
5��ѡ���� ��ȥ����������������������(������Ϊ����)����ѡ�õ��Լ��ͷ��뷽���ܴﵽʵ��Ŀ�ĵ���
| ѡ�� | ����� | �Լ� | ���뷽�� |
| A�� | ?�����飨�Ҵ��� | ��ʯ�� | ���� |
| B�� | ����(��ϩ�� | ���Ը��������Һ | ϴ�� |
| C�� | ������������ | ����ˮ | ��Һ |
| D�� | �����ᣨNaCl�� | ����ˮ | �ؽᾧ |