时间:2017-08-08 06:39:54
1、填空题 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如下图所示, 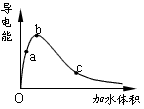
(1)O点导电能力为0的理由是___________________________________
(2)a、b、c三点溶液的c(H+)由小到大的顺序是___________________________________
(3)a、b、c三点醋酸的电离程度最大的是__________________________________
(4)要使c点c(CH3COO- )增大,c(H+)减少,可采取的措施是(至少写出三种方法)①_____________ ②___________________③__________________________
参考答案:
(1)在O点醋酸未电离,无自由离子存在
(2)c<a<b
(3) c
(4) ①加NaOH固体;②加少量的碳酸钠固体;③加入镁等金属;④醋酸钠固体
本题解析:
本题难度:一般
2、选择题 下列电离子方程式正确的是
A.NaHCO3=Na++H++CO32-
B.NaHSO4=Na++H++SO42-
C.H2SO4=2H++SO42-
D.KClO3=K++Cl-+3O2-
参考答案:BC
本题解析:略
本题难度:一般
3、选择题 H2A为弱电解质,0.1mol/LH2A水溶液加水稀释为0.01mol/L时,下列各粒子的浓度减小最多的是( )
A.A2-
B.HA-
C.H+
D.H2A
参考答案:H2A溶液中存在:H2A?HA-+H+,HA-?A2-+H+,加水稀释,促进电解质电离,n(H2A)减小,n(HA-)、n(H+)、n(A2-)增大,由于体积增大程度大于电离程度,则c(H2A)、c(HA-)、c(H+)、C(A2-)都减小,但溶液中还存在水的电离,则c(H+)>c(CH3COO-)>c(CH3COOH),根据Kw=c(H+)?c(OH-),可知c(OH-)浓度增大,
所以微粒浓度减小得最多的是H2A.
故选D.
本题解析:
本题难度:简单
4、选择题 下列物质中,不能电离出酸根离子的是
A.Na2SO4
B.Ba(OH)2
C.KMnO4
D.Na2CO3
参考答案:B
本题解析:
答案:B
B、电离出氢氧根离子,不是酸根;A、C、D分别电离出硫酸根、高锰酸根、碳酸根。
本题难度:一般
5、选择题 在含酚酞的0.1 mol/L氨水中加入少量NH4Cl晶体,则溶液颜色?(?)
A.变蓝色
B.变深
C.变浅
D.不变
参考答案:C
本题解析:氨水中存在电离平衡:NH3.H2O  ?NH4++OH- , 加入少量NH4Cl晶体,则增大了NH4+浓度,上述电离平衡将逆向移动,OH-浓度减小,故溶液颜色变浅
?NH4++OH- , 加入少量NH4Cl晶体,则增大了NH4+浓度,上述电离平衡将逆向移动,OH-浓度减小,故溶液颜色变浅
本题难度:一般