时间:2017-08-08 06:16:24
1、填空题 某化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数.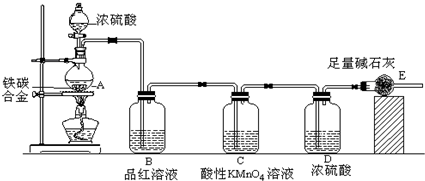
(1)m?g铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;②______.
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式______.
(3)B中的现象是:______;C的作用是:______.
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重b?g.则铁碳合金中铁的质量分数为______?(写表达式).
(5)甲同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:______.
(6)本套装置在设计上存在缺陷,其中导致测得铁的质量分数偏低的是(答一条即可)______.
参考答案:由装置图可知,该实验原理:通过测定干燥管E的质量增重确定二氧化碳的质量,根据二氧化碳的质量计算铁碳合金中碳的质量,进而计算铁的质量,再计算合金中铁的质量分数.故二氧化硫会影响二氧化碳的测定,进入干燥管E的气体应除去二氧化硫、且干燥.
(1)常温下,铁与浓硫酸反应生成一层致密的氧化物保护膜,阻止内金属继续与浓硫酸反应,发生钝化现象,
故答案为:常温下Fe遇浓硫酸发生钝化;
(2)碳与浓硫酸在加热的条件下生成二氧化硫、二氧化碳、水,反应方程式为C+2H2SO4(浓)?△?.?CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)?△?.?CO2↑+2SO2↑+2H2O;
(3)A中生成的气体含有CO2、2SO2,SO2具有漂白性,能使品红溶液褪色;
C装置的作用为除尽反应产物中的SO2气体,防止影响二氧化碳的质量测定,
故答案为:品红溶液褪色;除尽反应产物中的SO2气体;
(4)E增重b?g为二氧化碳的质量,根据碳元素守恒可知合金中碳元素的质量为1244bg,合金中铁的质量为mg-1244bg=(m-311b)g,故铁的质量分数(m-311b)gmg=11m-3b11m,
故答案为:11m-3b11m;
(5)装置内残留部分二氧化碳,未能被装置E完全吸收,导致测量的二氧化碳的质量偏小,即合金中碳元素的质量偏小,铁元素的质量增大,质量分数增大,
故答案为:装置内的CO2难以赶尽,导致E质量增重偏小;
(6)由装置图可知,SO2不一定能全部被品红KMnO4除去,E中碱石灰会吸收空气中的CO2、H2O等,
故答案为:SO2不一定能全部被品红KMnO4除去或E中碱石灰会吸收空气中的CO2、H2O等.
本题解析:
本题难度:一般
2、选择题 在吸收塔用98.3%的浓硫酸而不是用水吸收SO3的原因是( )
A.用浓硫酸吸收不形成酸雾,吸收速率快
B.用水吸收生成的酸雾多,影响吸收
C.用水不能吸收SO3
D.用浓硫酸吸收可以得到更浓的硫酸
参考答案:A
本题解析:
本题难度:简单
3、选择题 下列有关物质的性质和该性质的应用均正确的是
A.浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体
B.过氧化钠能与二氧化碳反应产生氧气,可用于高空飞行或潜水的供氧剂
C.油脂能在酸性溶液中水解生成高级脂肪酸,可用于防止油脂变质
D.铝的熔点很高,可用于制作耐高温材料
参考答案:B
本题解析:分析:A、浓硫酸和氨气反应不能干燥氨气;
B、过氧化钠和二氧化碳反应生成氧气,做供氧剂;
C、油脂变质是因为高级脂肪酸烃基中的不饱和键;
D、铝是活泼金属.
解答:A、浓硫酸具有吸水性,可用于干燥二氧化碳等气体,和氨气反应不能干燥氨气,故A错误;
B、过氧化钠能与二氧化碳反应产生氧气,人呼出的二氧化碳可以反应转化为氧气,可用于高空飞行或潜水的供氧剂,故B正确;
C、油脂变质是因为高级脂肪酸烃基中的不饱和键,故C错误;
D、氧化铝的熔点很高,可用于制作耐高温材料,铝是活泼金属,不能做耐高温材料,故D错误;
故选B.
点评:本题考查了化学知识的应用,浓硫酸吸水性,过氧化钠的氧化性,油脂结构分析,掌握基础是学习的关键,题目难度中等.
本题难度:一般
4、填空题 已知有机物A和C都是厨房中的常用调料品.A是一种无色,有特殊香味的液体,相对分子质量是氢气的23倍.A在Cu催化下,与氧气在加热条件下能生成有机物B;有机物C是一种有强烈刺激性气味的无色液体,能使紫色石蕊溶液变红,并且A与C可以生成一种有芳香气味的液体。
根据以上条件,写出下列反应的化学方程式(注明反应条件):
A→B:______________________________________________________
A+C:________________________________________________________
参考答案: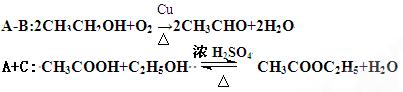
本题解析:略
本题难度:简单
5、选择题 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法不正确的是
[? ]
A. 该硫酸的物质的量浓度为18.4 mol/L
B. 配制500 mL 3. 68 mol/L的稀硫酸,需取该硫酸100.?0 mL
C. 该硫酸与等体积的水混合,所得溶液的质量分数大于49%
D. 该硫酸50 mL与足量的铜充分反应,可得到标准状况下SO2 20.6L
参考答案:D
本题解析:
本题难度:简单