时间:2017-08-08 04:59:18
1、选择题 纳米是长度单位,l nm="10" -9m,当物质的颗粒达到纳米级时,会具有一些特殊的性质。例如由铜制成“纳米铜”具有非常强的化学活性,在空气中可以燃烧。下列关于“纳米铜"的叙述正确的是
A.“纳米铜”比铜片的金属性强
B.“纳 米铜”比铜片更易失去电子
米铜”比铜片更易失去电子
C.“纳米铜"比铜片的氧化性强
D.“纳米铜”的还原性与铜片相同
2、填空题 (15分) 现代社会,铁合金可说是金属材料王国的霸主,铁广泛存在于铁的氧化物及多种矿石中,如下表所示:
| 矿石名称 | 磁铁矿 | 黄铁矿 | 赤铁矿 | 黄铜矿 |
| 主要成分 | Fe3O4 | FeS2 | Fe2O3 | CuFeS2 |
 2Fe2O3+8SO2,该反应中被氧化的元素是?,生成1molFe2O3转移电子的物质的量为?mol。
2Fe2O3+8SO2,该反应中被氧化的元素是?,生成1molFe2O3转移电子的物质的量为?mol。3、选择题 CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到。现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液。电解开始不久,阴极区溶液呈红色,而阳极区溶液呈蓝色,同时有白色沉淀生成。下列说法中正确的是
A.对阳极区溶液呈蓝色的正确解释是:2I--2e-=I2,碘遇淀粉变蓝
B.对阳极区溶液呈蓝色的正确解释是:Cu-2e-=Cu2+,Cu2+显蓝色
C.阴极区溶液呈红色的原因是:2H++2e-=H2↑,使阴极附近OH-浓度增大,溶液显碱性,从而使酚酞变红
D.阴极上的电极反应式为:Cu2++2e-=Cu
4、填空题 (10分)信息时代产生的大量电子垃圾对环境构成严重威胁。某研究性学习小组将一批废弃的线路板简单处理后,得到含Cu、Fe及少量Au、Pt等金属的混合物,并用如下流程制备胆矾晶体(CuSO4?5H2O):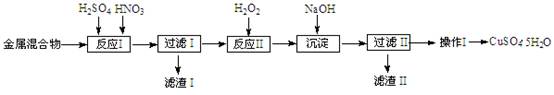 ?
?
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀 | 1.5 | 6.4 | 4.2 |
| 完全沉淀 | 3.2 | 8.9 | 6.7 |
 = 2Iˉ+S4O
= 2Iˉ+S4O
5、选择题 关于FeCl3进行的实验,下列预测正确的是?(?)
| 选项 | 实?验 | 预?测 |
| A | 蒸发FeCl3溶液 | 得到FeCl3固体 |
| B | 在FeCl3、CuCl2混合液中,加入少量Fe粉 | 一定有H2产生且有Cu析出 |
| C | 用FeCl3固体溶于水配制饱和溶液 | 会有Fe(OH)3沉淀产生 |
| D | 在FeCl3溶液中,加入KHCO3溶液 | 有CO2产生,但无Fe(OH)3沉淀生成 |