ʱ��:2017-08-08 04:53:18
1������� ij��ѧС�����������װ�ã��гֺͼ�����������ȥ������ⱥ��ʳ��ˮ�����õ�������H2��ԭCuO��ĩ���ⶨCu�����ԭ��������ͬʱ���������������ԣ�
��1��Dװ���е�ⱥ��ʳ��ˮ�����ӷ�Ӧ����ʽΪ��______
��2��Ϊ���������������ԣ���Eװ�õ���Һ������______��
A�����۵⻯����Һ?B������KMnO4��Һ?C��FeCl2��Һ?D��Na2S��Һ
��3��Fװ�õ�Ŀ����______��
��4��Ϊ�ⶨCu�����ԭ��������ijͬѧ��������µķ�����
��ȷ����Ӳ�ʲ����ܵ�����Ϊa?g������CuO��ȷ����Ӳ�ʲ����ܺ�CuO��������Ϊb?g��ʵ����Ϻ�ͨ����������������ͨ����ȷ����Ӳ�ʲ����ܺ�Cu�۵�������Ϊc?g������ȷ��Cu�����ԭ��������
�ٶ�Bװ���е�����ͭ��ĩ����ǰ����Ҫ���еIJ���Ϊ______��
��Aװ����ʢ�ŵ��Լ�Ϊ______��
�۸��ݲ�ý�����м��㣬��Cu�����ԭ������Ϊ______��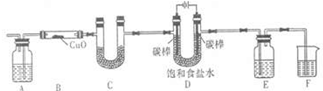
�ο��𰸣���1��Dװ���е�ⱥ��ʳ��ˮ�����������ơ���������������Ӧ���ӷ���ʽΪ2Cl-+2H2O?���?.?2OH-+H2��+Cl2����
�ʴ�Ϊ��2Cl-+2H2O?���?.?2OH-+H2��+Cl2����
��2�����������������ԣ�Ӧѡ��ԭ�����ʣ��ҷ�Ӧ�������ԣ�
A�����������⻯�أ����ɵⵥ�ʣ���Һ����ɫ����A��ȷ��
B������KMnO4��Һ������ǿ�����ԣ���B����
C����������FeCl2�����Ȼ�������Һ���ɫ����C��ȷ��
D����������Na2S��������Һ����ǣ���D��ȷ��
��ѡ��ACD��
��3�������ж�����Ⱦ������Fװ�õ�Ŀ��������δ��Ӧ����������ֹ��Ⱦ�������ʴ�Ϊ������δ��Ӧ��������
��4���������ǿ�ȼ�����壬��������ϣ�������������ըΣ�գ���������֮ͭǰҪͨ�������ž�װ���ڿ�����
�ʴ�Ϊ��ͨ�������ž�װ���ڿ�����
����װ��ͼ��ʵ��ԭ����֪��װ��A�������շ�Ӧ������ˮ������ˮ������ȷ������ͭ����Ԫ�ص���������A��ʢ�ŵ�ΪҺ�壬ӦΪŨ���ᣬ
�ʴ�Ϊ��Ũ���
������ͭ������Ϊ��b-a��g����Ӧ��ͭ������Ϊ��c-a��g��������ͭ����Ԫ�ص�����Ϊ��b-a��g-��c-a��g=��b-c��g����ͭ�����ԭ������Ϊx����x��16=��c-a��g����b-c��g�����x=16(c-a)b-c���ʴ�Ϊ��16(c-a)b-c��
���������
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ���ǣ�������
A��ͨ��ԭ��ؿ��Խ��κ���ʽ�Ļ�ѧ��ֱ��ת��Ϊ����
B��ԭ��صĸ����͵��ص������������ķ�Ӧͬ����������Ӧ
C���������������Һʱ������Ҫ����OH-����Һ��pH����С
D��̫���ܵ�ص���Ҫ�����Ǹߴ��ȵĶ�������
�ο��𰸣�A���������Զ�������������ԭ��Ӧ����Ϊ���ȷ�Ӧ������ԭ���ʵ�ֻ�ѧ��ת��Ϊ���ܣ���A����
B��ԭ��صĸ���ʧȥ���ӷ���������Ӧ�����ص�����ʧȥ���ӷ���������Ӧ����B��ȷ��
C���������������Һʱ��ʵ�ʵ��ˮ��OH-Ũ���������Ե������������Һʱ����Һ��pH��������C����
D��̫���ܵ�ص���Ҫ�����Ǹߴ��裬��������Ϊ���ά����Ҫԭ�ϣ���D����
��ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� ijЩʳƷ��װ������һ��С��������ע����˫����������ʳ�á���ͨ��������ѯ��֪����Ҫ�ɷ������ۡ�����̿���Ȼ��ơ�����������˫�����ķ����жϴ������
A�������������
B��������ʳƷ���ڵ�O2��N2
C����������ʱ������ԭ���ԭ��
D����Ϊ���ɫ��ʧЧ
�ο��𰸣�B
�����������ָ�ڿ����м�����������Ҳ������ˮ�ֵ����ʣ����������տ����е�������ˮ���������п��������ã���A��ȷ��˫�����ܹ����տ����е�O2��ˮ�������������տ����е�N2����B����˫������������ʱ������ԭ��ط�Ӧ������(C):2 H2O+O2+4e-=4OH- ����(Fe):Fe-2e-=Fe2+����C��ȷ������������Ϊ���ɫFe(OH)3�����ڼ����������������Ӧ����ʧЧ����D��ȷ��
�����Ѷȣ�һ��
4��ѡ���� ȫ�������ܵ�������ò�ͬ��̬���ӶԵ�������ԭ��Ӧ��ʵ�ֻ�ѧ�ܺ͵����ת����װ�ã�?��ԭ����ͼ��ʾ������H+�������Dz���������Ӧ����ͨ������Ĥ�����ƶ�ʹ�Ҳ���Һ���ֵ����ԡ������й�˵������ȷ���ǣ�?��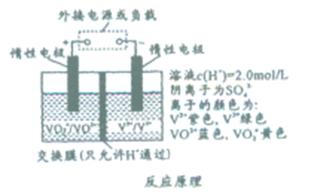
A���ŵ�ʱ�������Һ���ɻƱ�������缫��ӦʽΪ��VO2+ +eһ+2H+=VO2+ +H2O
B�����ʱ��ת�Ƶĵ�����Ϊ3��01��1023���������Һ��n��H+���ı仯��Ϊl��0mol
C�����ʱ��H+����۶����ƶ����Ҳ�
D���������У��Ҳ���Һ��ɫ������ɫ��Ϊ��ɫ
�ο��𰸣�B
���������A�����ڷŵ�ʱ�����Һ���ɻ�[VO2+]����[VO2+]���ݵ�ʧ�����غ���VO2+ +eһ�D�DVO2+���پݵ���غ���VO2+ +eһ+2H+�D�DVO2+������ԭ���غ��VO2+ +eһ+2H+=VO2+ +H2O��������ȷ�����ʱ�����Һ�з����ĵ缫��ӦΪVO2+��eһ+H2O=VO2+ +2H+����ת�Ƶĵ�����Ϊ3��01��1023�������� H+l.0mol��������H+ͨ������Ĥ���Ҳ��ƶ�����仯��С��l.0mol����B�����C����ȷ���ڳ������У��Ҳ�Ϊ����������缫��ӦΪV3++e-=V2+����Һ��ɫ������ɫ��Ϊ��ɫ��D����ȷ��
�����Ѷȣ�һ��
5��ѡ���� һ�������Ҵ�����û������������ܼ����ȼ״����Ч�ʸ߳�32��������ܷ�ӦΪ��C2H5OH +3O2�� 2CO2 +3H2O,���ʾ��ͼ����ͼ����������ֵ�ص�˵����ȷ����
A��b��Ϊ��صĸ���
B����ع���ʱ������a���ص��߾������ٵ�b��
C����������ĵ缫��ӦΪ��4H+ ��O2��4e����2H2O
D����״���£�ͨ��5.6LO2����ȫ��Ӧ����0.5mol����ת��
�ο��𰸣�BC
�����������
�����Ѷȣ�һ��