时间:2017-08-08 04:22:58
1、选择题 将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是
[? ]
A.稀硝酸?
B.稀盐酸
C.硝酸铜?
D.氢氧化钠
2、选择题 下列实验中产生现象与对应图形(纵坐标n均表示产生的Al(OH)3的物质的量)不相符的是
A.在AlCl3溶液中滴加氨水至过量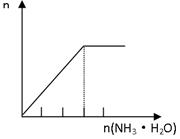
B.向NaOH溶液中滴加AlCl3至过量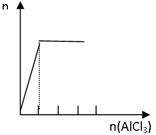
C.向NaAlO2溶液中滴加盐酸至过量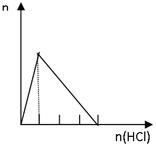
D.向H2SO4溶液中加入NaAlO2溶液至过量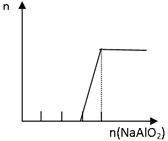
3、填空题 (12分)工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝。工艺流程如右图: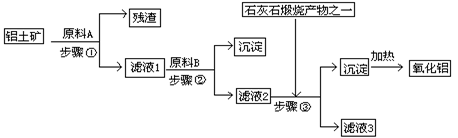
(1) 原料A的名称是____,步骤①反应的离子方程式是_________________。
(2) 滤液1中要加入稍过量原料B,原料B的化学式是__,步骤②反应的离子方程式是?
(3) 步骤③的化学方程式是:_____________________________________________。
(4) 如果省去步骤①,即溶解铝土矿是从加入原料B开始,后续操作不变,则会对氧化铝的提取有什么影响__________________________________________________。
4、选择题 向含 HCl 和 AlCl3的混合液中不断滴加 NaOH 溶液,下列图象中能正确表示上述反应的是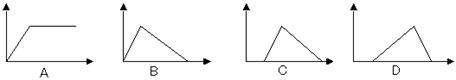
5、填空题 明矾石经处理后得到明矾[KAl(SO4)2・12H2O]。从明矾制备Al、K2SO4和H2SO4的工艺过程如下所示: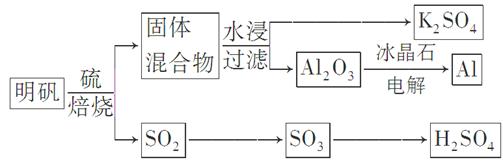 焙烧明矾的化学方程式为:4KAl(SO4)2・12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
焙烧明矾的化学方程式为:4KAl(SO4)2・12H2O+3S=2K2SO4+2Al2O3+9SO2↑+48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是________。
(2)从水浸后的滤液中得到K2SO4晶体的方法是________。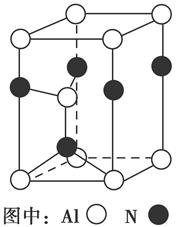
(3)Al2O3在一定条件下可制得AlN,其晶体结构如右图所示,该晶体中Al的配位数是________。
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是________。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:
2SO2(g)+O2(g) 2SO3(g) ΔH1=-197 kJ/mol;
2SO3(g) ΔH1=-197 kJ/mol;
H2O(g)=H2O(l) ΔH2=-44 kJ/mol;
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=-545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是________。焙烧948 t明矾(M=474 g/mol),若SO2的利用率为96%,可生产质量分数为98%的硫酸________t。